ЗАНЯТИЕ 5 10-й класс (первый год обучения)
Периодический закон и система химических элементов д.И.Менделеева План
1. История открытия периодического закона и системы химических элементов Д.И.Менделеева.
2. Периодический закон в формулировке Д.И.Менделеева.
3. Современная формулировка периодического закона.
4. Значение периодического закона и системы химических элементов Д.И.Менделеева.
5. Периодическая система химических элементов – графическое отражение периодического закона. Строение периодической системы: периоды, группы, подгруппы.
6. Зависимость свойств химических элементов от строения их атомов.
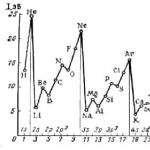
1 марта (по новому стилю) 1869 г. считается датой открытия одного из важнейших законов химии – периодического закона. В середине XIX в. было известно 63 химических элемента, и возникла потребность в их классификации. Попытки такой классификации предпринимали многие ученые (У.Одлинг и Дж.А.Р.Ньюлендс, Ж.Б.А.Дюма и А.Э.Шанкуртуа, И.В.Деберейнер и Л.Ю.Мейер), но лишь Д.И.Менделееву удалось увидеть определенную закономерность, расположив элементы в порядке возрастания их атомных масс. Эта закономерность имеет периодический характер, поэтому Менделеев сформулировал открытый им закон следующим образом: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины атомной массы элемента.
В системе химических элементов, предложенной Менделеевым, был ряд противоречий, которые сам автор периодического закона устранить не смог (аргон–калий, теллур–йод, кобальт–никель). Лишь в начале XX в., после открытия строения атома, был объяснен физический смысл периодического закона и появилась его современная формулировка: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.Такую формулировку подтверждает и наличие изотопов, химические свойства которых одинаковы, хотя атомные массы различны.
Периодический закон – один из основных законов природы и важнейший закон химии. С открытия этого закона начинается современный этап развития химической науки. Хотя физический смысл периодического закона стал понятен только после создания теории строения атома, сама эта теория развивалась на основе периодического закона и системы химических элементов. Закон помогает ученым создавать новые химические элементы и новые соединения элементов, получать вещества с нужными свойствами. Сам Менделеев предсказал существование 12 элементов, которые в то время еще не были открыты, и определил их положение в периодической системе. Свойства трех из этих элементов он подробно описал, и при жизни ученого эти элементы были открыты («экабор» – галлий, «экаалюминий» – скандий, «экасилиций» – германий). Кроме того, периодический закон имеет большое философское значение, подтверждая наиболее общие законы развития природы.
Графическим отражением периодического закона является периодическая система химических элементов Менделеева. Существует несколько форм периодической системы (короткая, длинная, лестничная (предложена Н.Бором), спиралеобразная). В России наибольшее распространение получила короткая форма. Современная периодическая система содержит 110 открытых на сегодняшний день химических элементов, каждый из которых занимает определенное место, имеет свой порядковый номер и название. В таблице выделяют горизонтальные ряды – периоды (1–3 – малые, состоят из одного ряда; 4–6 – большие, состоят из двух рядов; 7-й период – незавершенный). Кроме периодов выделяют вертикальные ряды – группы, каждая из которых подразделяется на две подгруппы (главную – а и побочную – б). Побочные подгруппы содержат элементы только больших периодов, все они проявляют металлические свойства. Элементы одной подгруппы имеют одинаковое строение внешних электронных оболочек, что обусловливает их схожие химические свойства.
Период – это последовательность элементов (от щелочного металла до инертного газа), атомы которых имеют одинаковое число энергетических уровней, равное номеру периода.
Главная подгруппа – это вертикальный ряд элементов, атомы которых имеют одинаковое число электронов на внешнем энергетическом уровне. Это число равно номеру группы (кроме водорода и гелия).
Все элементы в периодической системе разделяются на 4 электронных семейства (s -, p -, d -, f -элементы) в зависимости от того, какой подуровень в атоме элемента заполняется последним.
Побочная подгруппа – это вертикальный ряд d -элементов, имеющих одинаковое суммарное число электронов на d -подуровне предвнешнего слоя и s -подуровне внешнего слоя. Это число обычно равно номеру группы.
Важнейшими свойствами химических элементов являются металличность и неметалличность.
Металличность – это способность атомов химического элемента отдавать электроны. Количественной характеристикой металличности является энергия ионизации.
Энергия ионизации атома – это количество энергии, которое необходимо для отрыва электрона от атома элемента, т. е. для превращения атома в катион. Чем меньше энергия ионизации, тем легче атом отдает электрон, тем сильнее металлические свойства элемента.
Неметалличность – это способность атомов химического элемента присоединять электроны. Количественной характеристикой неметалличности является сродство к электрону.
Сродство к электрону – это энергия, которая выделяется при присоединении электрона к нейтральному атому, т. е. при превращении атома в анион. Чем больше сродство к электрону, тем легче атом присоединяет электрон, тем сильнее неметаллические свойства элемента.
Универсальной характеристикой металличности и неметалличности является электроотрицательность (ЭО) элемента.
ЭО элемента характеризует способность его атомов притягивать к себе электроны, которые участвуют в образовании химических связей с другими атомами в молекуле.
Чем больше металличность, тем меньше ЭО.
Чем больше неметалличность, тем больше ЭО.
При определении значений относительной ЭО по шкале Полинга за единицу принята ЭО атома лития (ЭО(Li) = 1); самым электроотрицательным элементом является фтор (ЭО(F) = 4).
В малых периодах от щелочного металла к инертному газу:
Заряд ядер атомов увеличивается;
Число энергетических уровней не изменяется;
Число электронов на внешнем уровне увеличивается от 1 до 8;
Радиус атомов уменьшается;
Прочность связи электронов внешнего слоя с ядром увеличивается;
Энергия ионизации увеличивается;
Сродство к электрону увеличивается;
ЭО увеличивается;
Металличность элементов уменьшается;
Неметалличность элементов увеличивается.
Все d -элементы данного периода похожи по своим свойствам – все они являются металлами, имеют мало различающиеся радиусы атомов и значения ЭО, поскольку содержат одинаковое число электронов на внешнем уровне (например, в 4-м периоде – кроме Cr и Cu).
В главных подгруппах сверху вниз:
Число энергетических уровней в атоме увеличивается;
Число электронов на внешнем уровне одинаково;
Радиус атомов увеличивается;
Прочность связи электронов внешнего уровня с ядром уменьшается;
Энергия ионизации уменьшается;
Сродство к электрону уменьшается;
ЭО уменьшается;
Металличность элементов увеличивается;
Неметалличность элементов уменьшается.
Периодический закон Д.И. Менделеева и периодическая система химических элементов имеет большое значение в развитии химии. Окунемся в 1871 год, когда профессор химии Д.И. Менделеев, методом многочисленных проб и ошибок, пришел к выводу, что «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». Периодичность изменения свойств элементов возникает вследствие периодического повторения электронной конфигурации внешнего электронного слоя с увеличением заряда ядра.
Современная формулировка периодического закона
такова:
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Преподавая химию, Менделеев понимал, что запоминание индивидуальных свойств каждого элемента, вызывает у студентов трудности. Он стал искать пути создания системного метода, чтобы облегчить запоминание свойств элементов. В результате появилась естественная таблица , позже она стала называться периодической .
Наша современная таблица очень похожа на менделеевскую. Рассмотрим ее подробнее.
Таблица Менделеева
Периодическая таблица Менделеева состоит из 8 групп и 7 периодов.
Вертикальные столбцы таблицы называют группами . Элементы, внутри каждой группы, обладают сходными химическими и физическими свойствами. Это объясняется тем, что элементы одной группы имеют сходные электронные конфигурации внешнего слоя, число электронов на котором равно номеру группы. При этом группа разделяется на главные и побочные подгруппы .
В Главные подгруппы входят элементы, у которых валентные электроны располагаются на внешних ns- и np- подуровнях. В Побочные подгруппы входят элементы, у которых валентные электроны располагаются на внешнем ns- подуровне и внутреннем (n — 1) d- подуровне (или (n — 2) f- подуровне).
Все элементы в периодической таблице , в зависимости от того, на каком подуровне (s-, p-, d- или f-) находятся валентные электроны классифицируются на: s- элементы (элементы главной подгруппы I и II групп), p- элементы (элементы главных подгрупп III — VII групп), d- элементы (элементы побочных подгрупп), f- элементы (лантаноиды, актиноиды).
Высшая валентность элемента (за исключением O, F, элементов подгруппы меди и восьмой группы) равна номеру группы, в которой он находится.
Для элементов главных и побочных подгрупп одинаковыми являются формулы высших оксидов (и их гидратов). В главных подгруппах состав водородных соединений являются одинаковыми, для элементов, находящихся в этой группе. Твердые гидриды образуют элементы главных подгрупп I — III групп, а IV — VII групп образуют а газообразные водородные соединения. Водородные соединения типа ЭН 4 – нейтральнее соединения, ЭН 3 – основания, Н 2 Э и НЭ — кислоты.
Горизонтальные ряды таблицы называют периодами . Элементы в периодах отличаются между собой, но общее у них то, что последние электроны находятся на одном энергетическом уровне (главное квантовое число n — одинаково).
Первый период отличается от других тем, что там находятся всего 2 элемента: водород H и гелий He.
Во втором периоде находятся 8 элементов (Li - Ne). Литий Li – щелочной металл начинает период, а замыкает его благородный газ неон Ne.
В третьем периоде, также как и во втором находятся 8 элементов (Na - Ar). Начинает период щелочной металл натрий Na, а замыкает его благородный газ аргон Ar.
В четвёртом периоде находятся 18 элементов (K - Kr) – Менделеев его обозначил как первый большой период. Начинается он также с щелочного металла Калий, а заканчивается инертным газом криптон Kr. В состав больших периодов входят переходные элементы (Sc - Zn) — d- элементы.
В пятом периоде, аналогично четвертому находятся 18 элементов (Rb - Xe) и структура его сходна с четвёртым. Начинается он также с щелочного металла рубидий Rb, а заканчивается инертным газом ксенон Xe. В состав больших периодов входят переходные элементы (Y - Cd) — d- элементы.
Шестой период состоит из 32 элементов (Cs - Rn). Кроме 10 d -элементов (La, Hf - Hg) в нем находится ряд из 14 f -элементов(лантаноиды)- Ce — Lu
Седьмой период не закончен. Он начинается с Франций Fr, можно предположить, что он будет содержать, также как и шестой период, 32 элемента, которые уже найдены (до элемента с Z = 118).
Интерактивная таблица Менделеева
Если посмотреть на периодическую таблицу Менделеева и провести воображаемую черту, начинающуюся у бора и заканчивающуюся между полонием и астатом, то все металлы будут находиться слева от черты, а неметаллы – справа. Элементы, непосредственно прилегающие к этой линии будут обладать свойствами как металлов, так и неметаллов. Их называют металлоидами или полуметаллами. Это бор, кремний, германий, мышьяк, сурьма, теллур и полоний.
Периодический закон
Менделеев дал следующую формулировку Периодического закона: «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Существует четыре основных периодических закономерности:
Правило октета
утверждает, что все элементы стремятся приобрести или потерять электрон, чтобы иметь восьмиэлектронную конфигурацию ближайшего благородного газа. Т.к. внешние s- и p-орбитали благородных газов полностью заполнены, то они являются самыми стабильными элементами.
Энергия ионизации
– это количество энергии, необходимое для отрыва электрона от атома. Согласно правилу октета, при движении по периодической таблице слева направо для отрыва электрона требуется больше энергии. Поэтому элементы с левой стороны таблицы стремятся потерять электрон, а с правой стороны – его приобрести. Самая высокая энергия ионизации у инертных газов. Энергия ионизации уменьшается при движении вниз по группе, т.к. у электронов низких энергетических уровней есть способность отталкивать электроны с более высоких энергетических уровней. Это явление названо эффектом экранирования
. Благодаря этому эффекту внешние электроны мене прочно связаны с ядром. Двигаясь по периоду энергия ионизации плавно увеличивается слева направо.

Сродство к электрону – изменение энергии при приобретении дополнительного электрона атомом вещества в газообразном состоянии. При движении по группе вниз сродство к электрону становится менее отрицательным вследствие эффекта экранирования.

Электроотрицательность — мера того, насколько сильно стремится притягивать к себе электроны связанного с ним другого атома. Электроотрицательность увеличивается при движении в периодической таблице слева направо и снизу вверх. При этом надо помнить, что благородные газы не имеют электроотрицательности. Таким образом, самый электроотрицательный элемент – фтор.

На основании этих понятий, рассмотрим как меняются свойства атомов и их соединений в таблице Менделеева.
Итак, в периодической зависимости находятся такие свойства атома, которые связанны с его электронной конфигурацией: атомный радиус, энергия ионизации, электроотрицательность.
Рассмотрим изменение свойств атомов и их соединений в зависимости от положения в периодической системе химических элементов .
Неметалличность атома увеличивается при движении в периодической таблице слева направо и снизу вверх . В связи с этим основные свойства оксидов уменьшаются, а кислотные свойства увеличиваются в том же порядке — при движении слева направо и снизу вверх. При этом кислотные свойства оксидов тем сильнее, чем больше степень окисления образующего его элемента
По периоду слева направо основные свойства гидроксидов ослабевают,по главным подгруппам сверху вниз сила оснований увеличивается. При этом, если металл может образовать несколько гидроксидов, то с увеличением степени окисления металла, основные свойства гидроксидов ослабевают.
По периоду слева направо увеличивается сила кислородосодержащих кислот. При движении сверху вниз в пределах одной группы сила кислородосодержащих кислот уменьшается. При этом сила кислоты увеличивается с увеличением степени окисления образующего кислоту элемента.
По периоду слева направо увеличивается сила бескислородных кислот. При движении сверху вниз в пределах одной группы сила бескислородных кислот увеличивается.
Категории ,Периодический закон Дмитрия Ивановича Менделеева - один из фундаментальных законов природы, который увязывает зависимость свойств химических элементов и простых веществ с их атомными массами. В настоящее время закон уточнен, и зависимость свойств объясняется зарядом ядра атома.
Закон был открыт русским ученым в 1869-м году. Менделеев представил его научному сообществу в докладе съезду Русского химического общества (доклад был сделан другим ученым, так как Менделеев был вынужден срочно выехать по заданию Вольного экономического общества Петербурга). В этом же году вышел учебник «Основы химии», написанный Дмитрием Ивановичем для студентов. В нем ученый описал свойства популярных соединений, а также постарался дать логическую систематизацию химических элементов. Также в нем впервые была представлена таблица с периодически расположенными элементами, как графическая интерпретация периодического закона. Всее последующие годы Менделеев совершенствовал свою таблицу, например, добавил столбец инертных газов, которые были открыты спустя 25 лет.
Научное сообщество далеко не сразу приняло идеи великого русского химика, даже в России. Но после того, как были открыты три новых элемента (галлий в 1875-м, скандий в 1879-м и германий в 1886-м годах), предсказанные и описанные Менделеевым в своем знаменитом докладе, периодический закон был признан.
- Является всеобщим законом природы.
- В таблицу, графически представляющую закон, включаются не только все известные элементы, но и те, которые открывают до сих пор.
- Все новые открытия не повлияли на актуальность закона и таблицы. Таблица совершенствуется и изменяется, но ее суть осталась неизменной.
- Позволил уточнить атомные веса и другие характеристики некоторых элементов, предсказать существование новых элементов.
- Химики получили надежную подсказку, как и где искать новые элементы. Кроме этого, закон позволяет с высокой долей вероятности заранее определять свойства еще неоткрытых элементов.
- Сыграл огромную роль в развитии неорганической химии в 19-м веке.
История открытия
Есть красивая легенда о том, что свою таблицу Менделеев увидел во сне, а утром проснулся и записал ее. На самом деле, это просто миф. Сам ученый много раз говорил, что созданию и совершенствованию периодической таблицы элементов он посвятил 20 лет своей жизни.
Все началось с того, что Дмитрий Иванович решил написать для студентов учебник по неорганической химии, в котором собирался систематизировать все известные на этот момент знания. И естественно, он опирался на достижения и открытия своих предшественников. Впервые внимание на взаимосвязь атомных весов и свойств элементов обратил немецкий химик Дёберейнер, который попытался разбить известные ему элементы на триады с похожими свойствами и весами, подчиняющимися определенному правилу. В каждой тройке средний элемент имел вес, близкий к среднему арифметическому двух крайних элементов. Ученый смог таким образом образовать пять групп, например, Li–Na–K; Cl–Br–I. Но это были далеко не все известные элементы. К тому же, тройка элементов явно не исчерпывала список элементов с похожими свойствами. Попытки найти общую закономерность позже предпринимали немцы Гмелин и фон Петтенкофер, французы Ж. Дюма и де Шанкуртуа, англичане Ньюлендс и Одлинг. Дальше всех продвинулся немецкий ученый Мейер, который в 1864-м году составил таблицу, очень похожую на таблицу Менделеева, но она содержала лишь 28 элементов, в то время как было известно уже 63.
В отличие от своих предшественников Менделееву удалось составить таблицу, в которую вошли все известные элементы, расположенные по определенной системе. При этом, некоторые клетки он оставил незаполненными, примерно вычислив атомные веса некоторых элементов и описав их свойства. Кроме этого, русскому ученому хватило смелости и дальновидности заявить, что открытый им закон является всеобщим законом природы и назвал его «периодическим законом». Сказав «а», он пошел дальше и исправил атомные веса элементов, которые не вписывались в таблицу. При более тщательной проверке, оказалось, что его исправления верны, а открытие описанных им гипотетических элементов стало окончательным подтверждением истинности нового закона: практика доказала справедливость теории.
составить таблицу, в которую вошли все известные элементы, расположенные по определенной системе. При этом, некоторые клетки он оставил незаполненными, примерно вычислив атомные веса некоторых элементов и описав их свойства. Кроме этого, русскому ученому хватило смелости и дальновидности заявить, что открытый им закон является всеобщим законом природы и назвал его «периодическим законом». Сказав «а», он пошел дальше и исправил атомные веса элементов, которые не вписывались в таблицу. При более тщательной проверке, оказалось, что его исправления верны, а открытие описанных им гипотетических элементов стало окончательным подтверждением истинности нового закона: практика доказала справедливость теории.
Периодический закон Д.И Менделеева.
Свойства химических элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости, от величины атомного веса.
Физический смысл периодического закона.
Физический смысл периодического закона заключается в периодичном изменении свойств элементов, в результате периодически повторяющихся e-ых оболочек атомов, при последовательном возрастании n.
Современная формулировка ПЗ Д.И Менделеева.
Свойство химических элементов, а также свойство образованных ими простых или сложных веществ находится в периодичной зависимости от величины заряда ядер их атомов.
Периодическая система элементов.
Периодическая система – система классификаций химических элементов, созданная на основе периодического закона. Периодическая система – устанавливает связи между химическими элементами отражающие их сходства и различия.
Периодическая таблица(существует два вида: короткая и длинная) элементов.
Периодическая таблица элементов – графическое отображение периодической системы элементов, состоит из 7 периодов и 8 групп.
Вопрос 10
Периодическая система и строение электронных оболочек атомов элементов.
В дальнейшем было установлено, что не только порядковый номер элемента имеет глубокий физический смысл, но и другие понятия, ранее рассмотренные ранее также постепенно приобретали физический смысл. Например, номер группы, указывая на высшую валентность элемента, выявляет тем самым максимальное число электронов атома того или иного элемента, которое может участвовать в образовании химической связи.
Номер периода, в свою очередь, оказался связанным с числом энергетических уровней, имеющихся в электронной оболочке атома элемента данного периода.
Таким образом, например, „координаты" олова Sn (порядковый номер 50, 5 период, главная подгруппа IV группы), означают, что электронов в атоме олова 50, распределены они на 5 энергетических уровнях, валентными являются лишь 4 электрона.
Физический смысл нахождения элементов в подгруппах различных категорий чрезвычайно важен. Оказывается, что у элементов, расположенных в подгруппах I категории, очередной (последний) электрон располагается на s-подуровне внешнего уровня. Эти элементы относят к электронному семейству. У атомов элементов, расположенных в подгруппах II категории, очередной электрон располагается на р-подуровне внешнего уровня. Это, элементы электронного семейства „р". Так, очередной 50-й электрон у атомов олова располагается на р-подуровне внешнего, т. е. 5-го энергетического уровня.
У атомов элементов подгрупп III категории очередной электрон располагается на d-подуровне , но уже пред внешнего уровня, это элементы электронного семейства «d». У атомов лантаноидов и актиноидов очередной электрон располагается на f-подуровне, пред пред внешнего уровня. Это элементы электронного семейства «f».
Не случайно, следовательно, отмеченные выше числа подгрупп этих 4-х категорий, то есть 2-6-10-14, совпадают с максимальными числами электронов на подуровнях s-p-d-f.
Но можно, оказывается, решить вопрос о порядке заполнения электронной оболочки и вывести электронную формулу для атома любого элемента и на основе периодической системы, которая с достаточной ясностью указывает уровень и подуровень каждого очередного электрона. Периодическая система указывает и на размещение одного за другим элементов по периодам, группам, подгруппам и на распределение их электронов по уровням и подуровням, потому что каждому элементу соответствует свой собственный, характеризующий его последний электрон. В качестве примера разберем составление электронной формулы для атома элемента циркония (Zr). Периодическая система дает показатели и „координаты" этого элемента: порядковый номер 40, период 5, группа IV, побочная подгруппа. Первые выводы: а) всех электронов 40, б) эти 40 электронов распределены на пяти энергетических уровнях; в) из 40 электронов только 4 являются валентными, г) очередной 40-й электрон поступил на d-подуровень пред внешнего, т. е. четвертого энергетического уровня. Подобные выводы можно сделать о каждом из 39 элементов, предшествующих цирконию, только показатели и координаты будут каждый раз иными.
1. Докажите, что Периодический закон Д. И. Менделеева, как и любой другой закон природы, выполняет объясняющую, обобщающую и предсказательную функции. Приведите примеры, иллюстрирующие эти функции у других законов, известных вам из курсов химии, физики и биологии.
Периодический закон Менделеева— один из основополагающих законов химии. Можно утверждать, что вся современная химия построена на нем. Он объясняет зависимость свойств атомов от их строения, обобщает эту зависимость для всех элементов, разделяя их на различные группы, а также предсказывает их свойства в зависимости от строения и строение в зависимости от свойств.
Существуют другие законы, несущие объясняющую, обобщающую и предсказательную функции. Например, закон сохранения энергии, закон преломления света, генетический закон Менделя.
2. Назовите химический элемент, в атоме которого электроны располагаются по уровням согласно ряду чисел: 2, 5. Какое простое вещество образует этот элемент? Какую формулу имеет его водородное соединение и как оно называется? Какую формулу имеет высший оксид этого элемента, каков его характер? Запишите уравнения реакций, характеризующих свойства этого оксида.
3. Бериллий раньше относили к элементам III группы, и его относительная атомная масса считалась равной 13,5. Почему Д. И. Менделеев перенес его во II группу и исправил атомную массу бериллия с 13,5 на 9?
Раньше элемент бериллий ошибочно относили к III группе. Причина этого заключалась в неправильном определении атомной массы бериллия (вместо 9 ее считали равной 13,5). Д. И. Менделеев предположил, что бериллий находится в II группе, основываясь на химических свойствах элемента. Свойства бериллия были очень похожи на свойства Mg и Ca, и совершенно не похожи на свойства Al. Зная, что атомные массы Li и В, соседних элементов к Be, равны соответственно 7 и 11, Д. И.Менделеев предположил, что атомная масса бериллия равна 9.
4. Напишите уравнения реакций между простым веществом, образованным химическим элементом, в атоме которого электроны распределены по энергетическим уровням согласно ряду чисел: 2, 8, 8, 2, и простыми веществами, образованными элементами № 7 и № 8 в Периодической системе. Каков тип химической связи в продуктах реакции? Какое кристаллическое строение имеют исходные простые вещества и продукты их взаимодействия?

5. Расположите в порядке усиления металлических свойств следующие элементы: As, Sb, N, Р, Bi. Обоснуйте полученный ряд, исходя из строения атомов этих элементов.
N, Р, As, Sb, Bi — усиление металлических свойств. Металлические свойства в группах усиливаются.
6. Расположите в порядке усиления неметаллических свойств следующие элементы: Si, Al, Р, S, Cl, Mg, Na. Обоснуйте полученный ряд, исходя из строения атомов этих элементов.
Na, Mg, Al, Si, P, S, Cl — усиление неметаллических свойств. Неметаллические свойства в периодах усиливаются.
7. Расположите в порядке ослабления кислотных свойств оксиды, формулы которых: SiO2, Р2O5, Al2O3, Na2O, MgO, Cl2O7. Обоснуйте полученный ряд. Запишите формулы гидроксидов, соответствующих этим оксидам. Как изменяется их кислотный характер в предложенном вами ряду?

8. Напишите формулы оксидов бора, бериллия и лития и расположите их в порядке возрастания основных свойств. Запишите формулы гидроксидов, соответствующих этим оксидам. Каков их химический характер?
9. Что такое изотопы? Как открытие изотопов способствовало становлению Периодического закона?
Периодическая система элементов отражает взаимосвязь химических элементов. Атомный номер элемента равен заряду ядра, численно он равен числу протонов. Число нейтронов, содержащихся в ядрах одного элемента, в отличие от числа протонов, может быть различным. Атомы одного элемента, ядра которых содержат разное число нейтронов, называются изотопами.
Каждый химический элемент имеет по несколько изотопов (природных или полученных искусственно). Атомная масса химического элемента равна среднему значению из масс всех его природных изотопов с учетом их распространенности.
С открытием изотопов для распределения элементов по периодической системе стали использовать заряды ядер, а не их атомные массы.
10. Почему заряды атомных ядер элементов в Периодической системе Д. И. Менделеева изменяются монотонно, т. е. заряд ядра каждого последующего элемента возрастает на единицу по сравнению с зарядом атомного ядра предыдущего элемента, а свойства элементов и образуемых ими веществ изменяются периодически?
Так происходит из-за того, что свойства элементов и их соединений зависят не от общего числа электронов, а только от валентных, которые находятся на последнем слое. Количество валентных электронов меняется периодически, следовательно, свойства элементов также меняются периодически.
11. Приведите три формулировки Периодического закона, в которых за основу систематизации химических элементов взяты относительная атомная масса, заряд атомного ядра и строение внешних энергетических уровней в электронной оболочке атома.
1. Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от относительных атомных масс элементов.
2. Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от заряда атомных ядер элементов.
3. Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от строения внешних энергетических уровней в электронной оболочке атома.