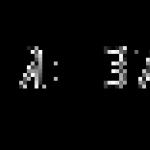1. Ilość ciepła wydzielanego podczas krzepnięcia ciała zależy od ...
A. Rodzaj substancji i jej masa.
B. Gęstość ciała i temperatura krzepnięcia.
W. Temperatury i wagi utwardzania.
G. Masa ciała, temperatura krzepnięcia i rodzaj substancji.
Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 500 g, ciepło właściwe topnienia
![]() . Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
. Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
2. Jaki odcinek wykresu charakteryzuje proces podgrzewania cieczy?
A. AB.B. Słońce.W. płyta CD.
A. 600°C.B. 650°C.W. 700°C.G. 750°C.D. 900°C.
A. 28 minutB. 10 minut.W. 6 minutG. 20 minut.D. 14 minut
A. 185 000 J
B. 185 000 000 J.
W. 740 J.
G. 740 000 J
D. 0,00135 J.
Opcja 2
1. Ilość ciepła przekazanego ciału podczas topienia wynosi ...
A.
Stosunek masy ciała do właściwego ciepła topnienia.
B.
B.

Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 150 g, ciepło właściwe topnienia
![]()
2. Która część wykresu charakteryzuje proces utwardzania?
A. AB.B. Słońce.W. płyta CD.
3. W jakiej temperaturze zakończyło się utwardzanie?
A.
1000°C.
B. 1400°C.
W. 1450°C.
G.
1500°C.
D.
1600°C.
A. 8 minutB. 5 minut.W. 13 minutG. 2 minuty.D. 15 minut.
A. 0,005 J
B. 45 000 000 J.
W.
2 000 000 J
G.
45 000 J
D. 2000 J.
Wykres topnienia i krzepnięcia ciał krystalicznych
Opcja 3
1. Kiedy substancja krystaliczna zestali się, ...
A. Więcej ciepła niż jest przez niego pobierane podczas topienia.B. Taka sama ilość ciepła jakpołknąć, gdy się rozpuści.
W. Mniejsza ilość ciepła, niż jest przez niego pobierana podczas topienia.

Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 250 g, ciepło właściwe topnienia
![]() . Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
. Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
2. Który odcinek wykresu charakteryzuje proces nagrzewania ciała stałego?
A. AB.B. Słońce.W. płyta CD.
3. W jakiej temperaturze zakończyło się topienie?
A.
30°C.B.
140°C.W.
160°C.G.
180°C.D.
200°C.
4. Jak długo ciało się topiło?
A. 18 minutB. 42 minutyW. 30 minut.G. 24 minutyD. 8 minut
5. Ile ciepła zużyto na proces topienia?
A. 0,58 J
B. 1720 J.
W.
107 500 J.
G.
1 720 000 J
D. 107 500 000 J.
Wykres topnienia i krzepnięcia ciał krystalicznych
Opcja 4
1. Ilość ciepła wydanego na stopienie ciała zależy od ...
A. Gęstość ciała i temperatura topnienia.
B. Masa ciała, temperatura topnienia i rodzaj substancji.
W. Temperatura topnienia i masy.
G. Rodzaj substancji i jej masa.

Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 200 g, ciepło właściwe topnienia
![]() . Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
. Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
2. Jaki odcinek wykresu charakteryzuje proces chłodzenia cieczą?
A. AB.B. Słońce.W. płyta CD.
3. W jakiej temperaturze rozpoczęło się utwardzanie?
A. 1200°C.W. 3400°C.D. 4800°C.
B.
3000°C.G.
3500°C.
4. Jak długo ciało stwardniało?
A. 24 minutyB. 10 minut.W. 18 minutG. 6 minutD. 8 minut
5. Ile ciepła wydzieliło się podczas procesu utwardzania?
A. 37 000 000 J.G. 925 J.
B. 925 000 JD. 37 000 J
W.
0,00108 J
Wykres topnienia i krzepnięcia ciał krystalicznych
Opcja 5
1. Ilość ciepła uwolnionego podczas krzepnięcia ciała wynosi ...
A. Iloczyn masy ciała i ciepła właściwego topnienia.
B. Stosunek ciepła właściwego topnienia do masy ciała.
W. Stosunek masy ciała do właściwego ciepła topnienia.

Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 400 g, ciepło właściwe topnienia
![]() . Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
. Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
2. Jaki odcinek wykresu charakteryzuje proces topienia?
A. AB.B. Słońce.W. płyta CD.
3. W jakiej temperaturze rozpoczęło się topienie?
A. 10°C.B. 20°C.W. 250°C.G. 270°C.D. 300°C.
4. Jak długo ciało się topiło?
A. 6 minutB. 11 minutW. 4 minutyG. 7 minutD. 14 minut
5. Ile ciepła zużyto na proces topienia?
A. 0,008 J
B. 20 000 J
W.
125 J.
G.
20 000 000 J.
D. 125 000 J
Wykres topnienia i krzepnięcia ciał krystalicznych
Opcja 6
1. Ciepło właściwe topnienia to ilość ciepła potrzebna do ...
A. Ogrzewanie stałej krystalicznej substancji o masie 1 kg do temperatury topnienia.
B. Przekształcenie w ciecz stałej substancji krystalicznej w temperaturze topnienia.
W. Przemiana w temperaturze topnienia stałej substancji krystalicznej o masie 1 kg w ciecz.

Rysunek przedstawia wykres zmian temperatury ciała w czasie. Masa ciała 750 g, ciepło właściwe topnienia
![]() . Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
. Po obejrzeniu zdjęcia odpowiedz na pytania 2-5.
2. Jaki odcinek wykresu charakteryzuje proces chłodzenia ciała stałego?
A. AB.B. Słońce.W. płyta CD.
3. W jakiej temperaturze rozpoczęło się utwardzanie?
A.
520°C.B.
420°C.W.
410°C.G.
400°C.D.
80°C.
4. Jak długo ciało stwardniało?
A. 6 minutB. 28 minutW. 10 minut.G. 12 minutD. 18 minut
5. Ile ciepła wydzieliło się podczas procesu utwardzania?
A. 160 000 JW. 160 J.D. 0,00626 J.
B. 90 000 000 JG. 90 000 J
Wykres topnienia i krzepnięcia
ciała krystaliczne

Test. Topienie i krzepnięcie ciał krystalicznych(praca z wykresami)
Opcja I
I. Jaka była temperatura ciała podczas pierwszej obserwacji?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
IV. W jakiej temperaturze rozpoczął się proces topienia?
1. Zwiększone.
2. Zmniejszone.
3. Nie uległo zmianie.
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
Opcja II

II. Jaki proces na wykresie charakteryzuje odcinek AB?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
III. Jaki proces na wykresie charakteryzuje odcinek BC?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
1. Zwiększone.
2. Zmniejszone.
3. Nie uległo zmianie.
VII. Jaki proces na wykresie charakteryzuje segment CD?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
VIII. Jaką temperaturę miało ciało podczas ostatniej obserwacji?
Opcja III
Rysunek przedstawia wykres ogrzewania i topnienia ciała krystalicznego.

I. Jaka była temperatura ciała w chwili pierwszej obserwacji?
1. 400°C. 2. 110°C. 3. 100°C.
4. 50°C. 5. 440°C.
II. Jaki proces na wykresie charakteryzuje odcinek AB?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
III. Jaki proces na wykresie charakteryzuje odcinek BC?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie.
IV. W jakiej temperaturze rozpoczął się proces topienia?
V. Jak długo ciało się topiło?
VI. Czy temperatura ciała zmieniła się podczas topnienia?
1. Zwiększone.
2. Zmniejszone.
3. Nie uległo zmianie.
VII. Jaki proces na wykresie charakteryzuje segment CD?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie
VIII. Jaką temperaturę miało ciało podczas ostatniej obserwacji?
Opcja IV
Rysunek przedstawia wykres chłodzenia i krzepnięcia ciała krystalicznego.

I. Jaką temperaturę miało ciało podczas pierwszej obserwacji?
II. Jaki proces na wykresie charakteryzuje odcinek AB?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie
III. Jaki proces na wykresie charakteryzuje odcinek BC?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie
IV. W jakiej temperaturze rozpoczął się proces utwardzania?
V. Jak długo ciało stwardniało?
VI. Czy temperatura ciała zmieniła się podczas hartowania?
1. Zwiększone.
2. Zmniejszone.
3. Nie uległo zmianie.
VII. Jaki proces na wykresie charakteryzuje segment CD?
1. Ogrzewanie.
2. Chłodzenie.
3. Topienie.
4. Utwardzanie
VIII. Jaką temperaturę miało ciało podczas ostatniej obserwacji?
„Zjawiska termiczne. Agregacyjne stany skupienia „Klasa 8.
Opcja 1.
A.1. Ołów topi się w temperaturze 327o C. Co można powiedzieć o temperaturze krzepnięcia ołowiu? 1) jest równa 327o C;
2) jest poniżej temperatury topnienia;
3) jest powyżej temperatury topnienia;
A.2. W jakiej temperaturze rtęć staje się krystaliczna?
1) 420o C; 4) 0oC;
2) -39o C;o C.
A.3. W ziemi na głębokości 100 km temperatura wynosi około 1000°C. Który z metali jest w stanie niestopionym?
1) cynk; 2) cyna; 3) żelazo.
A.4. Gaz opuszczający dyszę samolotu odrzutowego ma temperaturę 500–700° C. Czy dysza może być wykonana z aluminium?
1 może; 2) nie mogę.
A.5. Jaka była temperatura ciała w pierwszej chwili obserwacji?
A.6.
1) ogrzewanie; 3) topienie;
A.7
1) ogrzewanie; 3) topienie;
2) chłodzenie; 4) hartowanie.
A.8. W jakiej temperaturze rozpoczął się proces topienia?
1) 50o C;o C;o C.
2) 100o C;o C;
A.9. Jak długo ciało się topiło?
1) 8min; 3) 12min; 5) 7min.
2) 3 minuty; 4) 16 minut;
A.10. Czy podczas topnienia zmieniła się temperatura ciała?
A.11.
1) ogrzewanie; 3) topienie;
2) chłodzenie; 4) hartowanie.
A.12.?
1) 50o C;o C;o C.
2) 500°С; 4) 40o C;
A.13. Cząsteczki w kryształach zlokalizowane są:
A.14. Podczas ogrzewania ciał średnia prędkość ruchu cząsteczek:
A.15. Co można powiedzieć o energii wewnętrznej wody o masie 1 kg. w temperaturze
0o C i lód o masie 1 kg w tej samej temperaturze?
1) energia wewnętrzna wody i lodu jest taka sama;
2) lód ma dużą energię wewnętrzną;
3) woda ma dużą energię wewnętrzną.
A.16. Jaka energia jest potrzebna do stopienia 1 kg ołowiu w temperaturze 327°C?
1) 0,84*105J; 3) 5,9 * 106 J; 5) 2,1 * 106 J.
2) 0,25*105 J; 4) 3,9 * 106 J;
A.17. Korpusy z aluminium, miedzi i cyny są podgrzewane do temperatury topnienia każdego z nich. Który z nich wymaga więcej ciepła do stopienia, jeśli ich masy są takie same?
1) aluminium; 3) miedź.
2) cyna;
A.18. Podczas dryfowania lodu w pobliżu rzeki temperatura powietrza jest……….. niż poza nią. Wyjaśnia to fakt, że energia………..topnienia lodu.
1) powyżej... ... wyróżnia się; 3) wyższe…wchłonięte;
2) poniżej…. wyróżnia się; 4) poniżej…wchłonięty;
A.19. Jaka energia jest potrzebna do stopienia 1 kg żelaza w temperaturze topnienia?
1) 2,5 * 105 J; 3) 8,4 * 105 J; 5) 3,9 * 105 J.
2) 2,7*105 J; 4) 5,9 * 105 J;
A.20. Jaka energia jest potrzebna do stopienia 5 kg żelaza w temperaturze topnienia?
1) 2,3*105 J; 3) 7,8 * 106 J; 5) 1,35*106 J.
2) 2,0*105 J; 4) 6,2*105 J;
A.21.Stal otrzymywana jest poprzez przetapianie złomu w piecach martenowskich. Jaka energia jest potrzebna do stopienia złomu żelaza o masie 5 ton i temperaturze 10°C? Za temperaturę topnienia przyjęto 1460°C.
1) 4,05*106J; 4) 1,47 * 106 J;
2) 3,99*106J; 5) 4,90 * 106 kJ.
3) 1,97*106J;
A.22.Parowanie nazywa się zjawiskiem:
1) przejście cząsteczek w parę z powierzchni i z wnętrza cieczy;
A.23.Parowanie następuje:
1) w temperaturze wrzenia;
2) w dowolnej temperaturze;
3) w określonej temperaturze dla każdej cieczy.
A.24. Jeżeli do cieczy nie dopływa energia z innych ciał, to podczas jej parowania temperatura:
1) nie ulega zmianie; 2) podwyżki; 3) maleje.
A.25. Energia wewnętrzna podczas parowania cieczy:
1) nie ulega zmianie; 2) podwyżki; 3) maleje.
A.26. W jakim stanie skupienia będzie cynk w temperaturze wrzenia rtęci i pod normalnym ciśnieniem atmosferycznym?
1) w postaci stałej; 2) w płynie; 3) w stanie gazowym.
A.27.Czy energia wewnętrzna wody o masie 1 kg w temperaturze 100°C jest równa energii wewnętrznej pary wodnej o masie 1 kg w tej samej temperaturze?
2) energia wewnętrzna pary jest większa od energii wewnętrznej wody o 2,3 * 106 J;
3) energia wewnętrzna pary jest mniejsza od energii wewnętrznej wody o 2,3 * 106 J;
W 1. Oblicz ilość ciepła potrzebną do zamiany 8 kg eteru w parę,
pobierane w temperaturze 10°C.
O 2. Jaka energia zostanie uwolniona podczas krzepnięcia 2,5 kg srebra, wziętego w temperaturze
topnienia i dalsze ochłodzenie do 160°C.
C.1. Jaka temperatura końcowa zostanie ustalona, jeśli 500 g lodu osiągnie temperaturę
0°C, zanurzyć w 4 litrach wody o temperaturze 30°C.
C.1.Ile drewna opałowego należy spalić w piecu, wydajność \u003d 40%, aby uzyskać śnieg z 200 kg,
pobierana w temperaturze 10°C, woda w temperaturze 20°C.
„Zjawiska termiczne. Agregacyjne stany skupienia” Klasa 8.
Opcja 2.
A.1. Gdy substancja krystaliczna topi się, jej temperatura wynosi:
1) nie ulega zmianie; 2) podwyżki; 3) maleje;
A.2. W jakiej temperaturze cynk może znajdować się w stanie stałym i ciekłym?
1) 420o C; 4) 0oC;
2) -39o C;o C.
3) 1300o C -1500oC;
A.3. Który z metali – cynk, cyna czy żelazo – nie stopi się w temperaturze miedzi?
1) cynk; 2) cyna; 3) żelazo.
A.4. Temperatura zewnętrznej powierzchni rakiety podczas lotu wzrasta do 1500oC-2000o C. Z jakiego metalu można wykonać zewnętrzne poszycie rakiety?
1) cyna; 3) stal;
2) miedź; 4) wolfram.
A.5 Jaka była temperatura w pierwszym momencie obserwacji?

A.6. Który proces na wykresie charakteryzuje odcinek AB?
1) ogrzewanie; 3) topienie;
2) chłodzenie; 4) hartowanie.
A.7.Jaki proces na wykresie charakteryzuje segment BV?
1) ogrzewanie; 3) topienie;
2) chłodzenie; 4) hartowanie.
A.8. W jakiej temperaturze rozpoczął się proces utwardzania?
1) 80o C;o C;o C.
2) 350o C;o C;
A.9. Jak długo trwa utwardzanie organizmu?
1) 8min; 3) 12min; 5) 7min.
2) 4 minuty; 4) 16 minut;
A.10. Czy temperatura ciała zmieniła się podczas utwardzania?
1) wzrosła? 2) zmniejszona; 3) nie uległa zmianie.
A.11. Jaki proces na wykresie charakteryzuje odcinek VG?
1) ogrzewanie; 3) topienie;
2) chłodzenie; 4) hartowanie.
A.12. Jaka była temperatura ciała w ostatnim momencie obserwacji ?
1) 10o C;oC;o C; 4) 40o C;o C.
A.13. Cząsteczki w stopionej substancji znajdują się:
1) w ścisłej kolejności; 2) w nieładzie.
A.14. Cząsteczki w stopionej substancji poruszają się dzięki……… siłom przyciągania molekularnego.
1) losowo, nie przebywając w określonych miejscach;
2) w pobliżu pozycji równowagi, trzymając;
3) w pobliżu pozycji równowagi, nie pozostając w określonych miejscach.
A.15. Co można powiedzieć o energii wewnętrznej stopionego i niestopionego ołowiu o masie 1 kg w temperaturze 327°C?
1) energia wewnętrzna jest taka sama;
2) energia wewnętrzna stopionego ołowiu jest większa niż energii wewnętrznej niestopionego ołowiu;
3) energia wewnętrzna niestopionego ołowiu jest większa niż energii stopionego ołowiu;
A.16. Jaka energia zostanie uwolniona podczas krzepnięcia aluminium o masie 1 kg w temperaturze 660°C?
1) 2,7*105J; 3) 0,25*105 J; 5) 2,1 * 105 J.
2) 0,84 * 105 J; 4) 3,9 * 105 J;
A.17. Do pomieszczenia o temperaturze powietrza 0°C wprowadzono lód o tej samej temperaturze. Czy lód się stopi?
1) będzie, ponieważ lód topi się w temperaturze 0°C;
2) nie będzie, ponieważ nie będzie dopływu energii;
3) będzie, ponieważ energia jest pożyczana od innych ciał.
A.18. Podczas obfitych opadów śniegu w zimie temperatura powietrza wynosi……….., ponieważ kiedy kropelki wody powstałe z chmur krzepną………..energia.
1) wzrasta……….pochłonięty;
2) zmniejsza się……….. wyróżnia się;
3) wznosi się… wyróżnia się;
4) zmniejsza się………..pochłonięty.
A.19. Jaka energia jest potrzebna do stopienia 1 kg cyny w temperaturze topnienia?
1) 0,25 * 105 J; 3) 0,84 * 105 J; 5) 3,9 * 105 J.
2) 0,94*105 J; 4) 0,59*105 J;
A.20. Jaka energia jest potrzebna do stopienia 4 kg cyny w temperaturze topnienia?
1) 2,36 * 105 J; 3) 7,8 * 107 J; 5) 4,7 * 105 J.
2) 2,0*105 J; 4) 6,2*105 J;
A.21.Jaka ilość ciepła jest potrzebna do stopienia miedzi o masie 2 ton i temperaturze 25°C? Przyjmuje się, że temperatura topnienia miedzi wynosi około C
1) 5,29 * 107 kJ; 3) 1,97*105 kJ;
2) 3,99*105 kJ; 4) 1,268*105 tys. J; 5) 3,53 * 106 kJ.
A.22.Kondensacja to zjawisko, w którym:
1) parowanie nie tylko z powierzchni, ale także z wnętrza cieczy;
2) przejście cząsteczek z cieczy do pary;
3) przejście cząsteczek z pary w ciecz;
A.23.Kondensacji pary towarzyszy………..energia.
1) wchłanianie; 2) izolacja;
A.24. W tej samej temperaturze ilość ciepła wydzielonego podczas skraplania………..ilość (ilość) ciepła pochłoniętego podczas parowania.
jeszcze 1; 2) mniej; 3) równe.
A.25. Do talerza i szklanki wlano wodę o tej samej masie. Z którego naczynia wyparuje szybciej w tych samych warunkach
1) z talerza; 2) ze szklanki; 3) to samo.
A.26. Czy woda wyparuje w otwartym naczyniu w temperaturze 0°C?
1) tak, parowanie zachodzi w dowolnej temperaturze;
2) nie, w temperaturze 0°C woda twardnieje;
3) nie odparowuje, tworzenie się pary następuje, gdy ciecz wrze.
A.27.Ciepło właściwe parowania rtęci 0,3*106 J/kg. To znaczy dla… energii.
1) konwersja rtęci 0,3 * 106 kg w parę w temperaturze wrzenia wymaga 1 J;
2) przemiana 1 kg rtęci w parę wodną w temperaturze wrzenia wymaga 0,3 * 106 J;
3) ogrzewanie do temperatury wrzenia i zamiana w pary rtęci o masie 1 kg
Wymagane jest 0,3 * 106 J.
W 1. Określ ilość ciepła uwalnianego podczas chłodzenia i dalej
krystalizacja wody o masie 2 kg. Początkowa temperatura wody wynosi 30°C.
O 2. Jaka ilość ciepła jest potrzebna do ogrzania 1 g ołowiu, ilość początkowa
którego temperatura wynosi 27oC.
C.1. Ile ciepła potrzeba, aby stopić 3 kg lodu
temperatura początkowa -20°C i podgrzanie powstałej wody do tej temperatury
C.2.W naczyniu z wodą o temperaturze 0°C wpuścili 1 kg stopnia Celsjusza
para wodna. Po pewnym czasie w naczyniu ustalono temperaturę 20°C.
Określ masę wody znajdującą się początkowo w naczyniu.
Kolokwium w klasie 8. z wynikami z I półrocza trwa 2 godziny akademickie.
Test składa się z trzech części:
1) część A – wybierz poprawną odpowiedź;
2) część B – rozwiąż problem;
3) część C - rozwiąż problem o zwiększonej złożoności.
Kryteria oceny:
1) za każde poprawnie wykonane zadanie z części A-1 pkt;
2) za poprawnie rozwiązane zadanie w części B – 2 punkty;
3) za poprawnie rozwiązane zadanie w części C – 3 punkty; jednocześnie rozwiązanie problemów można ocenić w częściach 1 punktu (wzory są napisane poprawnie, procesy są nazwane, pokazane są wykresy procesów itp.)
opcja 1 | Opcja 2 |
|
Stopień „5”- od 32 do 38 punktów;
„4”- od 24 do 31 punktów;
„3”- od 16 do 23 punktów;
„2”- 15 punktów.
Cele i zadania lekcji: doskonalenie umiejętności graficznego rozwiązywania problemów, powtarzanie podstawowych pojęć fizycznych na ten temat; rozwój mowy ustnej i pisemnej, logiczne myślenie; aktywizacja aktywności poznawczej poprzez treść i stopień złożoności zadań; wzbudzanie zainteresowania tematem.
Plan lekcji.
Podczas zajęć
Niezbędny sprzęt i materiały: komputer, projektor, ekran, tablica, program Ms Power Point, dla każdego ucznia : termometr laboratoryjny, probówka z parafiną, uchwyt na probówkę, szklanka z zimną i gorącą wodą, kalorymetr.
Kontrola:
Rozpocznij prezentację „klawiszem F5”, zatrzymaj – „klawiszem Esc”.
Zmiany wszystkich slajdów organizujemy poprzez kliknięcie lewym przyciskiem myszy (lub naciśnięcie klawisza strzałki w prawo).
Powrót do poprzedniego slajdu „strzałka w lewo”.
I. Powtórzenie studiowanego materiału.
1. Jakie znasz zbiorcze stany materii? (slajd 1)
2. Co decyduje o tym lub innym stanie skupienia substancji? (slajd 2)
3. Podaj przykłady występowania substancji w różnych stanach skupienia w przyrodzie. (slajd 3)
4. Jakie jest praktyczne znaczenie zjawisk przejścia materii z jednego stanu skupienia w drugi? (slajd 4)
5. Jaki proces odpowiada przejściu substancji ze stanu ciekłego do stanu stałego? (slajd 5)
6. Jaki proces odpowiada przejściu substancji ze stanu stałego w ciecz? (slajd 6)
7. Co to jest sublimacja? Daj przykłady. (slajd 7)
8. Jak zmienia się prędkość cząsteczek substancji podczas przejścia ze stanu ciekłego do stałego?
II. Nauka nowego materiału
Na lekcji będziemy badać proces topienia i krystalizacji substancji krystalicznej - parafiny i nakreślimy te procesy.
W trakcie wykonywania doświadczenia fizycznego dowiemy się, jak zmienia się temperatura parafiny podczas ogrzewania i chłodzenia.
Doświadczenie wykonasz zgodnie z opisami do pracy.
Przed rozpoczęciem pracy przypomnę Ci zasady bezpieczeństwa:
Podczas wykonywania prac laboratoryjnych należy zachować ostrożność i ostrożność.
Inżynieria bezpieczeństwa.
1. Kalorymetry zawierają wodę o temperaturze 60°C, należy zachować ostrożność.
2. Zachowaj ostrożność podczas obchodzenia się ze szklanymi naczyniami.
3. Jeżeli urządzenie ulegnie przypadkowemu uszkodzeniu, poinformuj o tym nauczyciela, nie usuwaj samodzielnie fragmentów.
III. Frontalny eksperyment fizyczny.
Na stołach uczniów znajdują się arkusze z opisem pracy (załącznik nr 2), według których wykonują doświadczenie, budują harmonogram procesu i wyciągają wnioski. (Slajdy 5).
IV. Konsolidacja badanego materiału.
Podsumowanie wyników eksperymentu czołowego.
Wnioski:
Po podgrzaniu parafiny w stanie stałym do temperatury 50°C temperatura wzrasta.
Podczas topienia temperatura pozostaje stała.
Gdy cała parafina się stopi, temperatura wzrasta w miarę dalszego ogrzewania.
Po ochłodzeniu ciekłej parafiny temperatura spada.
Podczas krystalizacji temperatura pozostaje stała.
Gdy cała parafina zestali się, temperatura spada w miarę dalszego chłodzenia.
Schemat strukturalny: „Topienie i krzepnięcie ciał krystalicznych”
(slajd 12) Pracuj według schematu.
| Zjawiska | Fakty naukowe | Hipoteza | Idealny obiekt | Wielkie ilości | Prawa | Aplikacja |
| Kiedy ciało krystaliczne topi się, temperatura się nie zmienia. Kiedy krystaliczne ciało stałe zestala się, temperatura się nie zmienia. |
Kiedy ciało krystaliczne topi się, energia kinetyczna atomów wzrasta, sieć krystaliczna ulega zniszczeniu. Podczas krzepnięcia energia kinetyczna maleje i powstaje sieć krystaliczna. |
Ciało stałe to ciało, którego atomy są uporządkowanymi punktami materialnymi (sieć krystaliczna), oddziałującymi na siebie siłami wzajemnego przyciągania i odpychania. | Q to ilość ciepła Ciepło właściwe topnienia |
Q = m - pochłonięty Q = m - wyróżnia się |
1. Aby obliczyć ilość ciepła 2. Do stosowania w inżynierii, metalurgii. 3. procesy termiczne w przyrodzie (topnienie lodowców, zamarzanie rzek zimą itp.) 4. Zapisz swoje przykłady. |
Temperaturę, w której ciało stałe przechodzi w stan ciekły, nazywa się temperaturą topnienia.
Proces krystalizacji będzie przebiegał także w stałej temperaturze. Nazywa się to temperaturą krystalizacji. W tym przypadku temperatura topnienia jest równa temperaturze krystalizacji.
Zatem topienie i krystalizacja to dwa symetryczne procesy. W pierwszym przypadku substancja pobiera energię z zewnątrz, w drugim oddaje ją otoczeniu.
Różne temperatury topnienia determinują zakres różnych ciał stałych w życiu codziennym i technologii. Metale ogniotrwałe służą do wykonywania żaroodpornych konstrukcji w samolotach i rakietach, reaktorach jądrowych i elektrotechnice.
Utrwalenie wiedzy i przygotowanie do samodzielnej pracy.
1. Rysunek przedstawia wykres ogrzewania i topnienia ciała krystalicznego. (Slajd)
2. Dla każdej z poniższych sytuacji wybierz wykres, który najdokładniej odzwierciedla procesy zachodzące z substancją:
a) miedź jest podgrzewana i topiona;
b) cynk podgrzewa się do 400°C;
c) topniejącą stearynę ogrzewa się do 100°C;
d) żelazo wzięte w temperaturze 1539°C podgrzewa się do 1600°C;
e) cynę podgrzewa się od 100 do 232°C;
f) aluminium podgrzewa się od 500 do 700°C.
Odpowiedzi: 1-b; 2-a; 3-calowe; 4-calowe; 5B; 6-d;
Wykres odzwierciedla obserwacje zmiany temperatury dwójki
substancje krystaliczne. Odpowiedz na pytania:
(a) O której godzinie rozpoczęły się obserwacje poszczególnych substancji? Jak długo to trwało?
b) Która substancja zaczęła się topić jako pierwsza? Która substancja stopiła się jako pierwsza?
c) Podaj temperaturę topnienia każdej substancji. Nazwij substancje, których wykresy ogrzewania i topnienia są pokazane.
4. Czy w aluminiowej łyżce można stopić żelazo?
5.. Czy można zastosować termometr rtęciowy na biegunie zimna, gdzie zanotowano najniższą temperaturę - 88 stopni Celsjusza?
6. Temperatura spalania gazów proszkowych wynosi około 3500 stopni Celsjusza. Dlaczego lufa pistoletu nie topi się po wystrzale?
Odpowiedzi: Nie jest to możliwe, ponieważ temperatura topnienia żelaza jest znacznie wyższa niż temperatura topnienia aluminium.
5. Nie jest to możliwe, ponieważ w tej temperaturze rtęć zamarznie, a termometr ulegnie awarii.
6. Ogrzanie i stopienie substancji wymaga czasu, a krótki czas spalania prochu nie pozwala na rozgrzanie lufy do temperatury topnienia.
4. Samodzielna praca. (Załącznik 3).
opcja 1
Rysunek 1a przedstawia wykres ogrzewania i topnienia ciała krystalicznego.
I. Jaka była temperatura ciała podczas pierwszej obserwacji?
1. 300°C; 2. 600°C; 3. 100°C; 4,50°C; 5.550°C.
II. Który proces na wykresie charakteryzuje odcinek AB?
III. Jaki proces na wykresie charakteryzuje segment BV?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
IV. W jakiej temperaturze rozpoczął się proces topienia?
1,50°C; 2. 100°C; 3. 600°C; 4. 1200°C; 5. 1000°C.
V. Jak długo ciało się topiło?
1. 8 minut; 2. 4 minuty; 3. 12 minut; 4. 16 minut; 5,7 minuty
VI. Czy temperatura ciała zmieniła się podczas topnienia?
VII. Jaki proces na wykresie charakteryzuje odcinek VG?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
VIII. Jaką temperaturę miało ciało podczas ostatniej obserwacji?
1,50°C; 2. 500°C; 3. 550 °С; 4,40°C; 5. 1100°C.
Opcja 2
Rysunek 101.6 przedstawia wykres chłodzenia i krzepnięcia ciała krystalicznego.
I. Jaką temperaturę miało ciało podczas pierwszej obserwacji?
1. 400°C; 2. 110°C; 3. 100°C; 4,50°C; 5. 440°C.
II. Który proces na wykresie charakteryzuje odcinek AB?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
III. Jaki proces na wykresie charakteryzuje segment BV?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
IV. W jakiej temperaturze rozpoczął się proces utwardzania?
1. 80°C; 2. 350°C; 3. 320°С; 4. 450°C; 5. 1000°C.
V. Jak długo ciało stwardniało?
1. 8 minut; 2. 4 minuty; 3. 12 min;-4. 16 minut; 5,7 minuty
VI. Czy temperatura ciała zmieniła się podczas hartowania?
1. Zwiększone. 2. Zmniejszone. 3. Nie uległo zmianie.
VII. Jaki proces na wykresie charakteryzuje odcinek VG?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
VIII. Jaka była temperatura ciała w czasie ostatniej obserwacji?
1. 10°C; 2. 500°C; 3. 350°C; 4,40°C; 5. 1100°C.
Podsumowanie wyników samodzielnej pracy.
1 opcja
I-4, II-1, III-3, IV-5, V-2, VI-3, VII-1, VIII-5.
Opcja 2
I-2, II-2, III-4, IV-1, V-2, VI-3, VII-2, VIII-4.
Materiał dodatkowy: Obejrzyj film: „Topnienie lodu w temperaturze t<0C?"
Doniesienia studentów na temat zastosowania topienia i krystalizacji w przemyśle.
Praca domowa.
14 podręczników; pytania i zadania do akapitu.
Zadania i ćwiczenia.
Zbiór problemów V. I. Lukashika, E. V. Iwanowej, nr 1055-1057
Bibliografia:
- Peryszkin A.V. Klasa fizyki 8. - M.: Drop 2009.
- Kabardin O. F. Kabardina S. I. Orlov V. A. Zadania końcowej kontroli wiedzy uczniów z fizyki 7-11. - M.: Oświecenie 1995.
- Lukashik V. I. Ivanova E. V. Zbiór problemów fizyki. 7-9. - M.: Oświecenie 2005.
- Burov V. A. Kabanov S. F. Sviridov V. I. Czołowe zadania eksperymentalne w fizyce.
- Postnikov AV Sprawdzanie wiedzy uczniów z fizyki 6-7. - M.: Oświecenie 1986.
- Kabardin OF, Shefer NI Oznaczanie temperatury krzepnięcia i ciepła właściwego krystalizacji parafiny. Fizyka w szkole nr 5 1993.
- Kaseta wideo „Szkolny eksperyment fizyczny”
- Zdjęcia ze stron.
BUDŻET KOMUNALNY OGÓLNA INSTYTUCJA EDUKACYJNA
SZKOŁA ŚREDNIA nr 3 kl. ARZGIR
POWIAT ARZGIR KRAJ STAWROPOLSKI
TEMAT LEKCJI:
ROZWIĄZANIE PROBLEMÓW NA TEMAT: „TOPIENIE I TWARDZENIE CIAŁ KRYSTALICZNYCH
nauczyciel fizyki MBOU szkoła średnia nr 3
Z. Arzgir, region Arzgir
Terytorium Stawropola
Kolesnik Ludmiła Nikołajewna
2016
Sekcja programu: „Zmiana zbiorczych stanów materii”
Temat lekcji: „Rozwiązywanie problemów na temat „Topienie i krzepnięcie ciał krystalicznych”.
Cele Lekcji:
edukacyjne: pogłębienie i utrwalenie wiedzy teoretycznej studentów na temat topienia i krzepnięcia ciał krystalicznych poprzez rozwiązywanie problemów
rozwijanie: aby rozwijać logiczne myślenie uczniów, naucz ich porównywać i identyfikować to, co wspólne i wyróżniające w badanych zjawiskach
edukacyjne: ukazanie poznawalności świata i jego wzorców
Typ lekcji: Lekcja praktycznego zastosowania wiedzy i umiejętności
Rodzaj lekcji: Lekcja rozwiązywania problemów
Sprzęt: ulotka, prezentacja
Metody i techniki: Werbalne, wizualne, częściowo wyszukiwanie
Podczas zajęć
Wystąpienie wprowadzające nauczyciela
Zacznijmy opowieść o cieple,
Zapamiętajmy wszystko, podsumujmy teraz
Nie doprowadzimy mózgów do stopienia
Trenujemy je aż do wyczerpania!
Jesteśmy w stanie pokonać każde wyzwanie
A przyjacielowi zawsze możemy pomóc!
Organizowanie czasu (gotowość do zajęć, sprawdzanie nieobecności).Nauczyciel wprowadza uczniów w temat lekcji, cele lekcji.
Niech ta lekcja przyniesie Wam radość z komunikowania się ze sobą, ze mną, a Wasze dobre odpowiedzi i znajomość fizyki sprawią radość wszystkim.
Pierwszy etap to testowanie i samobadanie oraz mówienie z miejsca przez dzieci.
Badanie: Topienie i krzepnięcie ciał krystalicznych.
1. Nazywa się przejście substancji ze stanu ciekłego do stanu stałegoA. Topienie.
B. Dyfuzja.
B. Hartowanie.
G. Przez ogrzewanie.
D. Chłodzenie.
2. Żeliwo topi się w temperaturze 1200 0 C. A co z temperaturą krzepnięcia żeliwa?
A. Może być kimkolwiek.
B. Równy 1200 0 Z.
B. Powyżej temperatury topnienia
D. Poniżej temperatury topnienia.
3. Jaki odcinek wykresu charakteryzuje proces nagrzewania ciała stałego?
A. AV.
B. Niedz.
B. Płyta CD
4. W jakich jednostkach mierzy się ciepło właściwe topnienia?
A. J / kg B. J / kg∙ O Z V. J. G. kg
5. Ilość ciepła wydzielanego podczas krzepnięcia ciała wynosi ...
A. Pracamasa ciała na właściwe ciepło topnienia.
B. Stosunek ciepła właściwego topnienia do masy ciała.
B. Stosunek masy ciała do właściwego ciepła topnienia.
1. Nazywa się przejście substancji ze stanu stałego do ciekłego
A. Chłodzenie.
B. Hartowanie.
B. Dyfuzja.
G. Przez ogrzewanie.
D. Topienie.
2. Cyna twardnieje w temperaturze 232 0 C. Co można powiedzieć o jego temperaturze topnienia?
A. Powyżej temperatury utwardzania
B. Może być kimkolwiek.
W. Rawna 232 0 Z.
D. Poniżej temperatury utwardzania
3. Który segment wykresu charakteryzuje proces utwardzania?
A. AV.
B. Niedz.
B. Płyta CD
4. Ciepło właściwe topnienia to ilość ciepła potrzebna do ...
A. Ogrzewanie stałej krystalicznej substancji o masie 1 kg do temperatury topnienia.
B. Przekształcenie w ciecz stałej substancji krystalicznej w temperaturze topnienia.
B. Przemiana w temperaturze topnienia stałej substancji krystalicznej o masie 1 kg w ciecz.
5. Który ze wzorów określa ilość ciepła potrzebną do stopienia substancji?
A B C D.
Samokontrola.
Sprawdź samodzielnie poprawność testu -otwarte odpowiedzi na tablicy i umieść + lub - obok odpowiedzi. A teraz zaznacz - według liczby poprawnych odpowiedzi.Opowiedz, kto otrzymał 5,3,4 i jakie błędy popełnił.
Drugi etap to praca frontalna z klasą.

1. Rysunek przedstawia wykres ogrzewania i topnienia ciała krystalicznego.
I. Jaka była temperatura ciała podczas pierwszej obserwacji?
1 . 300°С; 2. 600°C; 3. 100°C; 4,50°C; 5.550°C.
IIAB?
III. Jaki proces na wykresie charakteryzuje ten segmentBV?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
IV. W jakiej temperaturze rozpoczął się proces topienia?
1,50°C; 2. 100°C; 3. 600°C; 4. 1200°C; 5. 1000°C.
V. Jak długo trwało topienie ciała?
1. 8 minut; 2. 4 minuty; 3. 12 minut; 4. 16 minut; 5,7 minuty
VI. Czy temperatura ciała zmieniła się podczas topnienia?
1. Zwiększone. 2. Zmniejszone. 3. Nie uległo zmianie.
VII. Jaki proces na wykresie charakteryzuje ten segmentVG?
1. Ogrzewanie. 2. Chłodzenie. 3. Topienie. 4. Utwardzanie.
VIII. Jaką temperaturę miało ciało podczas ostatniej obserwacji?
50°С; 2. 500°C; 3. 550 °С; 4,40°C; 5. 1100°C.
Dwa tygle z taką samą ilością stopionego ołowiu schładzają się w różnych pomieszczeniach: ciepłym i zimnym. Na którym z wykresów zbudowano pomieszczenie ciepłe, a które zimne?

Trzeci etap- minuta wychowania fizycznego.Ćwiczenia łagodzące zmęczenie wzroku.
1. Zamknij oczy. Otwórz oczy (5 razy).
2. Okrągłe ruchy oczu. Nie obracaj głową (10 razy).
3. Nie odwracając głowy, spójrz jak najdalej w lewo. Nie mrugaj. Patrz przed siebie. Mrugnij kilka razy. Zamknij oczy i odpocznij. To samo po prawej stronie (2-3 razy).
4. Spójrz na dowolny obiekt przed sobą i obracaj głowę w prawo i w lewo, nie odrywając wzroku od tego obiektu (2-3 razy).
5. Spójrz przez okno w dal przez 1 minutę.
Czwarty etap to praca w grupach z tekstem z materiałów OGE (zadanie 20.21 OGE z fizyki.).
Dzieci z 3. biurka siadają na 1. i 2. biurku w swoim rzędzie, grupa na miejscu pracuje z tekstem z materiałów OGE. Tekst i pytania znajdują się na ulotkach.
Jak rozwiązania zamarzają
Jeśli roztwór dowolnej soli w wodzie zostanie ochłodzony, okaże się, że temperatura krystalizacji spadła. Kryształy pojawią się w cieczy dopiero w temperaturze kilka stopni poniżej zera. Temperatura krystalizacji zależy od stężenia roztworu. Im niższe, tym wyższe stężenie roztworu. Na przykład, gdy 45 kg soli kuchennej rozpuści się w 1 m3 wody, temperatura krystalizacji spadnie do -3°C. Najniższą temperaturę ma roztwór nasycony, czyli roztwór zawierający możliwie największą ilość rozpuszczonej soli. W tym przypadku spadek temperatury jest dość znaczny. Tak więc nasycony roztwór soli kuchennej w wodzie krystalizuje w temperaturze -21 ° C, a nasycony roztwór chlorku wapnia - w temperaturze -55 ° C. Zobaczmy jak przebiega proces krystalizacji. Gdy w roztworze pojawią się pierwsze kryształki lodu, stężenie roztworu wzrośnie. Wzrośnie względna liczba cząsteczek soli, wzrośnie zakłócenie procesu krystalizacji wody, a temperatura krystalizacji spadnie. Jeśli temperatura nie zostanie dalej obniżona, krystalizacja zatrzyma się. Wraz z dalszym spadkiem temperatury kryształy wody będą nadal tworzyć się, a roztwór stanie się nasycony. Dalsze wzbogacanie roztworu w rozpuszczoną substancję (solę) staje się niemożliwe, a roztwór natychmiast krzepnie. Jeśli weźmiemy pod uwagę zamrożoną mieszankę , widać, że składa się z kryształków lodu i kryształków soli. Zatem roztwór zamarza inaczej niż zwykła ciecz. Proces zamrażania rozciąga się na duży przedział temperatur.
Co się stanie, jeśli posypiesz solą jakąś zmrożoną powierzchnię? Odpowiedź na to pytanie jest dobrze znana woźnym: gdy tylko sól zetknie się z lodem, lód zacznie się topić. Aby zjawisko miało miejsce, konieczne jest oczywiście, aby temperatura zamarzania nasyconego roztworu soli była niższa od temperatury powietrza. Kiedy lód zmiesza się z solą, lód topi się, a sól rozpuszcza się w wodzie. Ale topnienie wymaga ciepła, a lód zabiera je z otoczenia. W rezultacie temperatura powietrza spada. Zatem dodanie soli do lodu powoduje spadek temperatury.
Zadania do tekstu
Pytania w pierwszym rzędzie:
Co dzieje się z temperaturą krystalizacji roztworu wraz ze wzrostem stężenia substancji rozpuszczonej?
Co dzieje się z temperaturą powietrza podczas topnienia lodu?
Pytania z drugiego rzędu:
Co się stanie, gdy lód zmiesza się z solą?
Jak przebiega proces zamrażania?
Pytania z trzeciego rzędu:
Co zapobiega zamarzaniu wody w roztworze?
Od czego zależy temperatura krystalizacji roztworu?
Wszystkie odpowiedzi dzieci omawiamy głośno
Piąty etap- rozwiązywanie problemów.
1. Przypomnij sobie rodzaje zadań związanych z topieniem.

2. Przypomnij sobie algorytm rozwiązywania problemów.
Algorytm rozwiązywania problemów obliczeń cieplnych
1. Przeczytaj uważnie stan problemu, zapisz go, używając ogólnie przyjętych oznaczeń literowych; Wyraź wszystkie wielkości w układzie SI.
2. Dowiedz się: a) pomiędzy którymi ciałami zachodzi wymiana ciepła; b) które ciała w procesie wymiany ciepła są chłodzone, a które ogrzewane; c) które procesy opisane w stanie problemu zachodzą przy uwalnianiu, a które przy pochłanianiu energii.
3. Narysuj graficznie procesy opisane w zadaniach.
4. Zapisz równanie służące do obliczenia oddanej i odebranej ilości ciepła.
5. Wykonaj obliczenia i oceń wiarygodność wyniku.
Notatka:
a) Przed rozwiązaniem problemu należy zwrócić uwagę na temperaturę, w jakiej znajduje się substancja proponowana w stanie problemu. Jeśli substancja została już pobranaw temperaturze topnienia , problem zostanie rozwiązany w jednym kroku:Q = λ M .
b) Jeśli substancja zostanie pobranaNie w temperaturze topnienia , wówczas problem rozwiązuje się w trzech krokach:
1) najpierw musisz określić, ile ciepła potrzeba do ogrzania substancji od temperatury początkowejT 1 aż do temperatury topnieniaT 2 według wzoru:
Q 1 = cm ( T 2 – T 1 );
2) następnie oblicz ilość ciepła potrzebną do stopienia substancji już w temperaturze topnienia:Q 2 = λ M ;
3) określić całkowitą ilość ciepłaQ ogólny = Q 1 + Q 2
3. Rozwiązywanie problemów z materiałów OGE z fizyki (1 osoba rozwiązuje je przy tablicy)
Zadanie. Jaka ilość ciepła jest potrzebna do stopienia kawałka ołowiu o masie 2 kg w temperaturze 27°C? (λ=0,25×10 5 J/kg, s=140J/(kg× O Z))
1) 50 kJ
2) 78 kJ
3) 84 kJ
4) 134 kJ
Rozwiązanie.
Po stopieniu ołów zostaje wchłonięty![]() ciepło, gdzie- ciepło właściwe topnienia ołowiu. Po podgrzaniu ciepło jest pochłanianeGdzieto ciepło właściwe ołowiu,T 2
=327
O C to temperatura topnienia ołowiu,T 1
=27
O C. Łącznie ciepło zostanie uwolnione podczas topienia i ogrzewania:
ciepło, gdzie- ciepło właściwe topnienia ołowiu. Po podgrzaniu ciepło jest pochłanianeGdzieto ciepło właściwe ołowiu,T 2
=327
O C to temperatura topnienia ołowiu,T 1
=27
O C. Łącznie ciepło zostanie uwolnione podczas topienia i ogrzewania:
0,25×10 5 ×2+140×2×(327-27)=50000+84000=1340000J.
Odpowiedź: 4.
Dodatkowe zadanie. Rysunek przedstawia wykres zależności temperatury od ilości ciepła otrzymanego dla substancji o masie 2 kg. Początkowo substancja była w stanie stałym. Wyznacz ciepło właściwe topnienia substancji.
1) 25 kJ/kg
2) 50 kJ/kg
3) 64 kJ/kg
4) 128 kJ/kg
Rozwiązanie.
Ciepło właściwe topnienia to ilość energii potrzebna do stopienia jednostki masy. Na wykresie topienie odpowiada przekrojowi poziomemu. Zatem,
Prawidłowa odpowiedź to numer 1.
Dom. Stanowisko:
1. Powtórz kroki 12-15
2. Praca z tekstem z materiału OGE z fizyki
Magia lodu.
Obserwuje się interesującą zależność pomiędzy ciśnieniem zewnętrznym a temperaturą zamarzania (topnienia) wody. Wraz ze wzrostem ciśnienia do 2200 atmosfer spada: wraz ze wzrostem ciśnienia na atmosferę temperatura topnienia spada o 0,0075 ° C. Wraz z dalszym wzrostem ciśnienia temperatura zamarzania wody zaczyna rosnąć: przy ciśnieniu 3530 atmosfer woda zamarza w temperaturze 17 ° C, przy 6380 atmosferach - w temperaturze 0 ° C i przy 20 670 atmosferach - w temperaturze 76 ° C. W tym drugim przypadku zaobserwowany zostanie gorący lód. Przy ciśnieniu 1 atmosfery po zamrożeniu objętość wody gwałtownie wzrasta (o około 11%). W zamkniętej przestrzeni proces taki prowadzi do powstania ogromnego nadciśnienia. Woda zamarza, rozbija skały, kruszy wielotonowe bloki. W 1872 roku Anglik Bottomley jako pierwszy odkrył eksperymentalnie zjawisko rozrzedzania lodu. Drut z zawieszonym na nim ładunkiem zostaje umieszczony na kawałku lodu. Drut stopniowo tnie lód już w temperaturze 0°C, jednak po przejściu przez drut nacięcie pokrywa się lodem, w wyniku czego kawałek lodu pozostaje nienaruszony. Przez długi czas uważano, że lód pod ostrzami łyżew topi się pod wpływem silnego ciśnienia, temperatura topnienia lodu spada - i lód się topi. Jednak obliczenia pokazują, że osoba ważąca 60 kilogramów, stojąc na łyżwach, wywiera na lód ciśnienie około 15 atmosfer. Oznacza to, że pod łyżwami temperatura topnienia lodu spada jedynie o 0,11 ° C. Taki wzrost temperatury zdecydowanie nie jest wystarczający, aby lód zaczął się topić pod naciskiem łyżew podczas jazdy na przykład w temperaturze -10 °C.
Zadania do tekstu
1. Jak temperatura topnienia lodu zależy od ciśnienia zewnętrznego?
2. Podaj dwa przykłady ilustrujące występowanie nadciśnienia podczas zamarzania wody.
3. Spróbuj wyjaśnić własnymi słowami, co może oznaczać termin „związek”.
4. W trakcie jakiego procesu może wydzielać się ciepło, które podczas jazdy na łyżwach służy do topienia lodu?
3. Jaka ilość ciepła zostanie wydzielona podczas krystalizacji 2 kg stopionej cyny, pobranej w temperaturze krystalizacji, a następnie jej ochłodzenia do 32°C?
1) 210 kJ 2) 156 kJ 3) 92 kJ 4) 14,72 kJ
Odbicie.