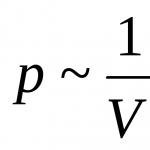· индекс ) Другие источники : МЭСБЕ
Бойля-Мариотта закон , связывающий изменения объема газа при постоянной температуре с изменениями его упругости. Этот закон, открытый в 1660 г. англ. физиком Бойлем и позже, но, независимо от него, Мариоттом во Франции, по своей простоте и определенности занимает весьма важное место в науке, хотя позднейшие исследования показали существование отступлений от него и что закон относится собственно к так называемому идеальному газу. История открытия его весьма поучительна. Франциск Лин (Franciscus Linus), профессор математики в Люттихе (1595-1675), не признавал, чтобы воздух, столь подвижное и легкое вещество, мог поддерживать ртутный столб в барометрической трубке, хотя ученик Галилея Евангелиста Торричелли (1608-1647) несомненно доказал, что именно давление атмосферы есть причина этого явления. До того времени все допускали, что природа не терпит пустоты (horror vacui) и что поэтому в пустые трубки устремляется ртуть, вода и вообще всякие жидкости. Когда же оказалось, что вода в трубке следует за поршнем насоса только до высоты несколько более 30 футов, то Галилей положил, что боязнь пустоты имеет предел. Лин же объяснял, что ртуть держится в трубке невидимыми нитями (funiculus) и что он сам чувствовал эти нити, когда закрывал пальцем верхнее отверстие трубки, которая была потом наполнена ртутью и опрокинута нижним концом в чашечку со ртутью же; при этом ртуть в достаточно длинной трубке опускалась, но останавливалась на известной высоте. Такое толкование опыта Торричелли Лином побудило Бойля сделать несколько новых опытов, которые им описаны в его «A defense of the doctrine touching spring and weight of the air» (Лондон, 1662). Чтобы доказать, что воздух обладает способностью сопротивления, Бойль взял сифонообразную трубку, запаянную на коротком конце (черт. 1). Когда в длинное колено наливали ртуть, то она сжимала воздух, заключенный в коротком колене, тем значительнее, чем более налито было ртути в другом. Когда ртуть в коротком колене доходила до уровня AB, в длинном она была на уровне CD, значит, упругость сжатого воздуха была такова, что он мог поддерживать давление ртутного столба высотою от AB до CD. А так как эта высота в первых опытах Б. была равна высоте ртути в барометре, то этим доказывалось, что в барометре ртутный столб поддерживался атмосферным воздухом. Наливая различные, все большие и большие количества ртути в длинное колено трубки, Б. записывал высоты ртутного столба и соответственные объемы сжатого воздуха, но сначала не обратил внимания на численные их соотношения. Его ученик Ричард Тоунлей (Richard Townley), просматривая числа таблицы, заметил, что объемы запертого воздуха обратно пропорциональны давлениям, на него производимым. Если воздух занимал сначала 12 дюймов длины в трубке, причем ртуть в обоих коленах была на одной высоте, то когда в длинное колено было прилито столько ртути, что воздух занял только 6 дюймов длины, оказалось, что высота поддерживаемого столба ртути была 29 англ. дюймов. Вначале воздух, запертый в коротком колене, имел упругость одинаковую с атмосферой, которая могла поддерживать в барометре ртуть на 29 дюймов высоты, а во втором случае запертый воздух подвержен был давлению атмосферы и давлению ртутного столба в 29 дюйм., т. е. в сумме - давлению 29 x 2 дюйма: значит, когда объем воздуха стал вдвое меньше, его упругость сделалась вдвое больше. После этого Бойль многократно повторял и разнообразил опыты и доказал, что тот же закон приложим к случаям увеличения объема воздуха.
Для этого он пользовался цилиндрическим сосудом (черт. 2), который был наполнен ртутью; погружая туда трубку А с открытыми концами до тех пор, пока над ртутью оставалась часть AB, длиною равная 1 дюйму, Б. закрывал и заклеивал отверстие А и затем поднимал трубку. При этом объем AB увеличивался и наконец обращался в объем AD - вдвое больший; ртуть же поднималась на высоту В"D, которая была почти вдвое менее, 29¾ дюйма, тогдашней высоты ртути в барометре. Очевидно, что воздух, заключавшийся в DA, не имел достаточной упругости, чтобы давить на поверхность D с такою силою, как он прежде давил на В; разность упругостей в обоих положениях трубки имеет мерою столб DB", которого длина оказалась 15⅜ дюйма. Поэтому упругость воздуха в удвоенном объеме AD составляет 29¾ без 15⅜, т. е. 14⅜ или почти ровно половину прежней. Когда трубка была поднята настолько, что объем AD занял длину в 10 дюймов, то высота ртути DB" оказалась в 26¾, следовательно, упругость воздуха измерялась разностью 29¾-26¾, т. е. 3 дюйма, что составляет почти точно 1 / 10 первоначальной упругости. Описание этих опытов находится в «New Experiments touching the spring of the air» (Оксф., 1660); «Continuation of Experiments» (Оксф., 1669), «On the rarefaction of air» (Лондон, 1671); «Second continuation» (Лондон, 1681), «General history of the air» (Лондон, 1692). Французский ученый Мариотт (Edme Mariotte, 1620-1684) произвел ряд опытов совершенно таким же образом и нашел тот же закон, который обыкновенно и называется его именем; только англичане называют его законом Бойля. См. сочинения Мариотта: «Essay sur la nature de l’Air» (Париж, 1676), «Du mouvement des eaux et des autres fluides» (part. II, disc. 2). Знал ли Мариотт об опытах Бойля - на это положительного ответа нельзя дать, хотя известно, что Мариотт находился в сношениях с английскими учеными уже в 1668 году. Как бы то ни было, Мариотт произвел такие же опыты и измерения, как и Бойль, только с большею точностью, и его опыты сделались более известны. Трубка (черт. 1) получила, как прибор, название Мариоттовой, и закон назван его именем, хотя с некоторого времени по справедливости его называют законом Бойля-Мариотта ; может быть, еще справедливее было бы присоединить имя и Тоунлея. Во всяком случае, Мариотт так известен своими другими трудами, что, несмотря на свидетельство цифр, трудно его подозревать в несамостоятельности работ, приведших ко вторичному открытию важного физического закона. История физики показывает, что очень важные законы, открытые в одной стране, могли долгое время быть неизвестными в другой; так, важный закон, касающийся силы гальванического тока, открытый Омом в Германии, был через несколько лет вторично открыт во Франции физиком Пулье.
С уменьшением объема воздуха вдвое-втрое необходимо увеличивается и плотность его в таком же отношении; температура газа при измерении его объема должна быть постоянною, а иначе охлаждение его или нагревание само по себе может изменить объем и упругость; кроме того, воздух не должен содержать воды или иных жидкостей. С соблюдением всех этих условий закон Бойля-Мариотта должен быть выражен таким образом: объемы некоторого определенного количества сухого воздуха при постоянной температуре обратно пропорциональны давлениям, на него производимым, а следовательно, и упругостям его , плотность же воздуха прямо пропорциональна этому давлению; или, вкратце, объем воздуха обратно пропорционален давлению, на него производимому. Если обозначить начальный объем газа буквою v, а давление, под которым он находится, - буквою р, если сжатый объем газа будет v", а давление, всегда измеряемое высотою ртутного столба, будет р"; то закон Б.-М. выразится пропорцией: v: v" = р":р; откуда pv = p"v", т. е. произведение объема газа на соответственное давление есть величина постоянная при не изменяющейся температуре. Другие газы, как будет объяснено далее, следуют тому же закону. Как ни просты кажутся опыты Бойля и Мариотта, однако и при той малой степени точности устройства приборов, какая была доступна в то время, они требовали соблюдения многих экспериментальных предосторожностей. Несоблюдение надлежащих правил было, вероятно, причиною различных разноречивых показаний позднейших наблюдателей. Например, Без наблюдал под экватором в своих опытах уменьшение объема воздуха в меньшем отношении, чем увеличение его упругости. Многочисленные опыты Бугара в тех же широтах, напротив, подтверждали закон Б.-М.; кроме того, опыты Амонтона, Сгравезанда, Фонтаны, Шукбурга привели к тому же заключению.
Но все опыты того времени не доходили до больших давлений и не были так точны, чтобы не оставалось сомнений в верности закона. Зульцер («Mém. de Berlin», т. IX, 1753), а потом и Робизон заключили из своих опытов, что при давлениях, в 7 или 8 раз превосходивших атмосферное, упругость увеличивается в значительно меньшем отношении, чем уменьшается объем; но опыты Винклера (1765) опять доказывают приложимость закона Б.-М. до 8 атмос. давления. В нынешнем столетии (1826) датские ученые Эрстедт со Свенсеном еще раз подтвердили верность закона до 8 атм. давления; другие их опыты, простиравшиеся до 70 атмосф., сделаны по методе, менее заслуживающей доверия. Но и в этих недалеких пределах (до 8 атм) некоторые газы не следуют закону Б.-М. Во второй половине XVIII стол. Ван Марум удостоверился, что аммиачный газ уменьшается в объеме гораздо быстрее воздуха; подобное тому Эрстедт и Свендсен гораздо позже нашли для газа сернистой кислоты. Вдобавок было открыто, что и тот и другой газы при несколько большем давлении переходят в жидкое состояние; это свойство потом было доказано и для других газов. Депре (Despretz) еще более точными опытами («Ann. de Chim. et de phys.», 2, XXXIV, 1827) убедился, что очень многие газы не следуют закону Б.-М. даже при таких давлениях, которые далеки от тех, при которых происходит сжижение газов. Депре делал опыты по способу, сходному с употребленным впервые Ван Марумом. Две стеклянные, с одного конца запаянные трубки, из которых одна была наполнена воздухом, а другая иным газом, были погружены открытыми концами в наполненную ртутью ванночку, помещенную на дне стеклянного цилиндра, наполненного водою. Давление производилось на воду посредством поршня, помещенного в верхнем дне цилиндра, вода давила на ртуть, которая, входя в трубочки, сжимала газы. Опыты, сделанные таким прибором, привели Депре к заключению, что аммиачный, сернистый, сероводородный и синеродистый газы при одинаковой величине давления занимают меньший объем, чем воздух. Точность измерений была настолько велика, что разность между сжатием этих газов и воздуха была заметна уже при уменьшении объема последнего только вдвое; при этом объемы названных газов составляли менее половины начального объема. По опытам Депре, водородный газ сжимается одинаково с воздухом до 1 / 15 первоначального объема, но при двадцати атмосферах давления объем водорода был более соответственного объема воздуха. Дюлонг и Араго («Mémoires de l’Académie des Sciences», т. X, «Annales de Chim. et de Phys.», т. XLIII, 1830) измеряли сжатие воздуха до 27 атмосфер давления; их прибор состоял из трубки длиною в 1,7 м, в которой был сжимаем воздух, и соединенной с ней другой, составленной из 13 частей, каждая в 2 метра длины. Эта длинная составная трубка была прикреплена к деревянной мачте, установленной внутри высокой башни. Дюлонг и Араго нашли, что закон Б.-М. верен для воздуха даже при сжатии его до 1 / 24 первоначального объема. Позже французский физик Пулье делал опыты по способу, сходному с тем, которым пользовались Эрстедт и Депре, но при больших давлениях, и заключил, что кислород, азот, водород, окись углерода и окись азота следуют до 100 атмосфер тому же закону сжатия, как и воздух, но что шесть нижепоименованных газов сжимаются более воздуха и что разность между их объемами и объемом воздуха растет с увеличением давления. Эти газы суть: сернистая кислота, аммиак, углекислота, закись азота, маслородный и болотный газы.
В 1847 г. были опубликованы («Mémoires de l’Académie des sciences de Paris», XXI, 1847) обширные и точные исследования Реньо по этому предмету, которые вместе с прочими физическими работами, исполненными по поручению французского правительства, описаны в указанных мемуарах под заглавием «Relation des expériences entreprises par ordre de M. le ministre des travaux publics etc». Воспользовавшись усовершенствованиями в приборах и способах наблюдения, введенными его предшественниками, Реньо прибавил новые существенные улучшения, устранив главное затруднение в точности измерения постепенно уменьшающихся объемов газа. Как ни значительна была длина трубки, в которой сжимался газ в опытах Араго и Дюлонга (1,7 метра), все же при сильных давлениях объем газа становился очень малым, и тогда всякая маленькая неточность в измерении положения ртути, запирающей газ, становится все более и более ощутительною относительно измеряемого постоянно уменьшающегося объема. Реньо употребил в своих опытах трубку в 3 метра длины для сжатия газов и после измерения полного объема газа и потом сжатого до половины объема при некотором соответственном давлении снова накачивал в эту трубку газ до совершенного ее наполнения. Полученный таким образом опять большой объем газа, находившийся под давлением, бо льшим первоначального, был приводим опять к половинному объему посредством увеличения высоты ртутного столба в длинной трубке. Пользуясь этим способом, Реньо при весьма больших давлениях (для 25 атмосфер для воздуха) измерял всегда большие объемы; кроме того, он принял во внимание много других экспериментальных предосторожностей, обеспечивших ему точность заключений. Опытами Реньо доказано, что важный закон природы, указанный Бойлем и Мариоттом, не формулируется математически точно теми простыми отношениями, которые они дали ему, что сжатие или уменьшение объема воздуха и азота происходит в несколько большем отношении, чем увеличение давления на газ или чем упругости последнего, и что для водорода сжатие, напротив, несколько слабее, чем бы следовало ожидать в случае точной применимости к нему закона Б.-М. Несколько чисел, взятых из мемуаров Реньо, помещенных в следующей табличке, показывают, что замеченные отступления вообще малы, но явно возрастают с увеличением давления. В первых двух столбцах таблицы показаны высоты давящего на газ ртутного столба, выраженные в атмосферах (у Реньо в миллиметрах), причем мерою нормального давления атмосферы принимается высота в 760 млн. ртутного столба. Цифры третьего столбца показывают частные, полученные от разделения отношения первоначального объема газа к объему, уменьшенному сжатием, на отношение последнего давления к первоначальному. Если назвать буквами v, v 1 объемы газа первоначальный и уменьшенный, а букв. р и р 1 - соответственные давления на газ, то по закону Б.-М. должно быть: v: v 1 = р 1: р, отсюда (v: v 1): (р 1: р) = 1, т. е., если оба написанные отношения действительно равны, то частное от разделения одного отношения на другое должно быть равно 1. Но цифры третьего столбца все больше 1 и медленно, но постоянно возрастают:
Всякое число третьего столбца показывает частное, относящееся к уменьшению объема воздуха вдвое при переходе давления от р (число первого столбца) к р 1 (втор. столб.). Из этих чисел видно, что уменьшение объема воздуха происходит в большем отношении, чем возрастание соответственного давления или упругости газа. Сначала оба отношения мало отличаются между собою, но при переходе от 12 атм. к 24 уменьшение объема в 1,006366 раз значительнее увеличения давления. Небольшое вычисление позволяет заключить, что 10000 куб. сант. воздуха при давлении в 0,972 атм, будучи подвергнуты давлению в 24,9 раз большему, займут объем в 396 куб. сант. вместо 401 к. с., как бы то следовало, если б закон Б.-М. точным образом выражал закон природы.
Сжатие азота представляет подобные же, но несколько меньшие отступления от закона Б.-М., а так как атмосферный воздух состоит из кислорода и азота, то Реньо заключил, что кислород сжимается более, чем азот и воздух. Следующая табличка содержит в себе числа, полученные при опытах I с водородом; цифры столбцов имеют то же значение, как и в таблице А.
Так как все числа третьего столбца меньше единицы и постоянно уменьшаются, то объем сжатого водорода постоянно более, чем бы то следовало по закону Б.-М., и с увеличением давления это отступление возрастает. По уподоблению Реньо, водород сжимается как пружина, все меньше и меньше с возрастанием давления. Что же касается углекислого газа, сравнительно легко сжимающегося, который представляет, подобно воздуху, более быстрое уменьшение объема, чем увеличение упругости, то он отступает от закона уже при сравнительно слабых давлениях при обыкновенной температуре, но, будучи нагрет до температуры кипения воды (100° Ц.), показывает гораздо меньшие отступления. Если из чрезвычайно точных опытов Реньо и следует заключить, что закон Б.-М. с весьма неощутительными отступлениями применяется только к некоторым газам при давлениях, далеких от точки сжижения, и при значительно высокой температуре, то этими результатами изучение вопроса не исчерпывается. Опыты Бойля и Реньо разделены промежутком времени без малого в 200 лет. Свойства газов изучены во многих отношениях в этот промежуток времени, список сжижающихся газов постоянно увеличивался, а несколько лет тому назад трудами Пикте и Кальете (Cailletet) сделано окончательное обобщение, что с уменьшением объема газов посредством давления и с понижением их температуры все они обращаются в жидкость. Вместе с тем исследования над сжатием газов пополнены другими учеными, которые сжимали газ давлениями, далеко превосходящими 25 и 30 атмосфер, на которых остановился Реньо и его ближайшие предшественники. Было упомянуто выше, что уже Пулье доводил давления до 100 атм., но его опыты не так были расположены, чтобы в них можно было найти ответ на значение закона Б.-М. при высоких давлениях. Такой ответ дают опыты Наттерера, Кальете и Амага для сильных давлений и опыты Д. И. Менделеева - для слабых. Амага установил свой прибор на дне шахты, имевшей около 400 метров (около 190 саж.) глубины. Измерения объема газа на такой глубине и огромной высоты давящего ртутного столба сопровождались такими большими техническими затруднениями, что непосредственно была изучена сжимаемость только азота. Закон сжатия других газов по сравнению с азотом был найден Амага по способу Депре и Пулье. В опытах Амага давление достигало 430¾ атмосферы, причем объем азота уменьшился только в 335¾ раза. Кальете опускал свой прибор в артезианский колодец глубиною в 500 метров (около 230 саж.); высота давящего ртутного столба постепенно была увеличиваема по мере опускания прибора. Трубка, в которой сжимался газ, была внутри вызолочена; ртуть, входя в нее, амальгамировала золото, так что на позолоте оставался след, предел между газом и ртутью, по которому и можно было измерять объем, занятый сжатым газом. Кроме того, Кальете производил опыты над сжиманием воздуха и водорода в особом приборе, в котором давления доводились до 605 атмосфер. Этим опытам предшествовали еще исследования Наттерера (1851-1854), который при помощи особого устройства нагнетательного насоса доводил давление на газ до 2790 атмосфер. Газ был сгущаем в толстостенном стальном сосуде, который был снабжен хорошо сделанным клапаном, постепенно нагружаемым по мере увеличения упругости газа, которая и измерялась весом груза на клапане. По окончании сжатия газа он был перепускаем по частям в другой сосуд определенного объема, где он принимал упругость, равную одной атмосфере, причем определялось последовательное уменьшение упругости сжатого газа, сначала быстрое, потом все более и более замедлявшееся. Числа, полученные при этих измерениях, дали средство определить упругости газов, соответственные его сжатию. Совокупность всех этих опытов по сравнению с опытами Реньо привела к тому заключению, что все газы, за исключением водорода, подвергаются таким изменениям объема v и упругости р, начиная с одной атмосферы, что произведение vp уменьшается, пока давление или упругость не достигнет некоторого предела, и что с дальнейшим увеличением давления это произведение vp увеличивается. В первом периоде газы сжимаются более, чем следует по закону Б.-М., во втором периоде - менее. Пределы, т. е. число атмосфер давления, при котором величина сжатия должна получаться согласно закону Б.-М., показаны различными исследователями не одинаково, но несомненно, что для каждого газа есть особый такой предел; только водород при всех испытанных давлениях сжимается меньше, чем следует по закону Б.-М. Оставалось пополнить эти исследования еще изучением связи между упругостью и объемом газов при давлениях, меньших атмосферного, т. е. в разреженном воздухе; по малоточным опытам Бойля и Мариотта, и для разреженного воздуха их закон верен. Точное исследование закона сжатия разреженных газов сделано Д. И. Менделеевым при сотрудничестве М. Л. Кирпичева (опыты Императорского русского технического общества, «Об упругости газов» Д. Менделеева, часть 1, СПб., 1875, in 4°). Эта работа и другие, к ней соприкасающиеся, были произведены на средства Технического общества; на те же средства было напечатано названное сочинение, в котором описаны приемы и приборы автора для измерения упругости и объемов газов. Опыты были произведены над воздухом, водородом и углекислотою. Ниже помещен один ряд опытов, из которых видны соотношения между объемами весьма разреженного воздуха и его упругостью.
Отсюда видно, что с уменьшением давления на газ его объем увеличивается в меньшем отношении, чем уменьшается упругость, следоват., и наоборот: с увеличением давления объем уменьшается в меньшем отношении. В самом деле: второе давление в 7,71 раза менее первого, а второй объем только в 7,38 раза более первого; третье давление в 2,35 раза менее второго, а третий объем в 1,92 раза более второго. Значит, сжатие и расширение воздуха при весьма малых давлениях отступает от закона Б.-М. в ту же сторону, как при весьма сильных давлениях; подобное тому получилось и для углекислоты. По этому же вопросу работали Амага и Зильештром, Реньо тоже сделал несколько измерений с воздухом при упругости в 300 миллим. Реньо и Зильештром пришли к тому заключению, что разреженный воздух отступает от закона Б.-М. в ту же сторону, как и при давлениях несколько выше атмосферного; опыты Амага не привели его к достоверным результатам (см. критическую оценку опытов Р. и З., сделанную Д. И. Менделеевым в сочинении «Об упругости газов», §§ 82, 92, 94.)
Резюмируя все сказанное относительно воздуха, можно видеть, что в разреженном состоянии он сжимается менее , чем следует по закону Б.-М., что при плотности около атмосферной и большей ее воздух сжимается более , чем по закону Б.-М., и, наконец, при весьма большой плотности он опять отступает в ту же сторону, как при весьма малой. При переходе от отступлений в одну сторону к отступлениям в другую воздух необходимо должен сжиматься согласно закону Б.-М., и это происходит всего два раза в пределах от наименьшей исследованной упругости (около ⅓ милл.) до наибольшей (2700 атмосфер). Другие газы, вероятно, следуют тому же закону переменного сжатия, кроме водорода, который постоянно сжимается менее, чем по закону Б.-М.
Давно уже были возбуждены сомнения о том, чтобы газы могли следовать закону Б.-М. при весьма сильных давлениях. Так как при сжатии плотность газа постоянно в такой же мере увеличивается, то можно бы дойти до того, что сжатый газ был бы плотнее самого плотного металла, т. е. что газ, доведенный сжатием до некоторого объема, был бы тяжелее, напр., платины, взятой в том же объеме. Беспредельного уплотнения газа нельзя допустить по той причине, что вещество газа, само по себе занимающее некоторую часть пространства, тем самым поставляет предел сжатию. Новейшая химия (см. Менделеев, «Об упругости газов», стр. 8-12) приводит к соображениям, которые не позволяют допустить, чтобы газ сжатием мог быть доведен до весьма большой плотности. А в действительности замеченный факт, что все испытанные газы при больших давлениях занимают объем не столь малый, как бы следовало по закону Б.-М., и что отступления от этого закона тем значительнее, чем больше давление; этот факт показывает, что уменьшение объема приближается к некоторому пределу. Для некоторых газов при обыкновенной температуре такой предел найден, так как эти газы обращаются в жидкость, а жидкости при самых сильных давлениях лишь весьма незначительно уменьшаются в объеме. Другие газы, не обращающиеся в жидкость от одного сжатия без более или менее значительного понижения температуры, все более и более отступают от закона Б.-М. Водород при 3000 атм. давления занимает объем только в 1000 раз меньший первоначального, т. е. при этом давлении его объем втрое более, чем можно бы ожидать в случае точности закона Б.-М. Несколько опытов Реньо над сжатием газов при температуре кипения воды показывают, что при возвышении температуры отступления от закона Б.-М. становятся менее; это обстоятельство привело его к заключению, что возвышение температуры приближает газ к идеальному состоянию, в котором он следует закону Б.-М., но такое понятие об идеальном газе еще не довольно обосновано. В заключение надо сказать, что закон Б.-М., собственно выражая сжатие газов только в некоторых предельных случаях, тем не менее послужил исходной точкой для изучения их свойств. Вместе с законом Гей-Люссака, относящимся к расширению газов от теплоты, он представляет математическую формулу, которую нужно видоизменить, чтобы представить во всей полноте явления изменения объема газов. Формула Ван дер Вальса (см. это слово) уже глубже проникает в натуру газов.
Несмотря на множество экспериментальных работ над сжатием газов, наука может ожидать еще новых, еще более обширных исследований. Точные и трудные исследования весьма расширенных газов, сделанные Д. И. Менделеевым, ведущие к важным заключениям, желательно бы видеть повторенными и распространенными. Опыты Реньо останутся надолго руководящими, но точность нашего времени может показаться недостаточной в ближайшем будущем.
Изменение одного из макроскопических параметров вещества определенной массы - давления р, объема V или температуры t - вызывает изменение остальных параметров.
Если одновременно меняются все величины, характеризующие состояние газа, то на опыте трудно установить какие-либо определенные закономерности. Проще сначала изучить процессы, в которых масса и один из трех параметров - р, V или t - остаются неизменными. Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами.
Закон Бойля-Мариотта
Первый газовый закон был открыт английским ученым Р. Бойлем (1627-1691) в 1660 г. Работа Бойля называлась «Новые эксперименты, касающиеся воздушной пружины». И действительно, газ ведет себя подобно сжатой пружине, в этом можно убедиться, сжимая воздух в обычном велосипедном насосе.
Бойль изучал изменение давления газа в зависимости от объема при постоянной температуре. Процесс изменения состояния термодинамической системы при постоянной температуре называют изотермическим (от греческих слов isos - равный, therme - тепло). Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой с большой системой, в которой поддерживается постоянная температура, - термостатом. Термостатом может служить атмосферный воздух, если температура его заметно не меняется на протяжении опыта.
Бойль наблюдал за изменением объема воздуха, запертого в длинной изогнутой трубке столбом ртути (рис. 3.6, а). Вначале уровни ртути в обоих коленах трубки были одинаковыми и давление воздуха равно атмосферному (760 мм рт. ст.). Доливая ртуть в длинное колено трубки, Бойль заметил, что объем воздуха уменьшился вдвое, когда разность уровней в обоих коленах оказалась равной h = 760 мм, и, следовательно, давление воздуха увеличилось вдвое (рис. 3.6, б). Это навело Бойля на мысль о том, что объем данной массы газа и его давление находятся в обратно пропорциональной зависимости.
а) б)
Дальнейшие наблюдения за изменением объема при доливании различных порций ртути подтвердили это заключение.
Независимо
от Бойля несколько позднее французский
ученый Э. Мариотт (1620-1684) пришел к тем
же выводам. Поэтому найденный закон
получил название закона
Бойля-Мариотта.
Согласно этому закону давление данной
массы (или количества) газа при постоянной
температуре обратно пропорционально
объему газа:
 .
.
Если p 1 - давление газа при объеме V 1 , и p 2 - его давление при объеме V 2 , то
 (3.5.1)
(3.5.1)
Отсюда следует, что p 1 V l = p 2 V 2 , или
 (3.5.2)
(3.5.2)
при t = const.
Произведение давления газа данной массы на его объем постоянно, если температура не меняется.
Этот закон справедлив для любых газов, а также для смесей газов (например, для воздуха).
Убедиться в справедливости закона Бойля-Мариотта можно с помощью прибора, изображенного на рисунке 3.7. Герметичный гофрированный сосуд соединен с манометром, регистрирующим давление внутри сосуда. Вращением винта можно менять объем сосуда. Об объеме можно судить с помощью линейки. Меняя объем и измеряя давление, можно заметить, что уравнение (3.5.2) выполняется.

Как и другие физические законы, закон Бойля-Мариотта является приближенным. При давлениях, в несколько сотен раз больших атмосферного, отклонения от этого закона становятся существенными.
На графике зависимости давления от объема каждому состоянию газа соответствует одна точка.
Изотермы
Процесс изменения давления газа в зависимости от объема изображается графически с помощью кривой, которая носит название изотермы (рис. 3.8). Изотерма газа выражает обратно пропорциональную зависимость между давлением и объемом. Кривую такого рода называют гиперболой. Разным постоянным температурам соответствуют различные изотермы, так как более высокой температуре при одном и том же объеме соответствует большее давление*. Поэтому изотерма, соответствующая более высокой температуре t 2, лежит выше изотермы, соответствующей более низкой температуре t 1.
* Подробнее об этом будет рассказано в дальнейшем.

Формулировки
Утверждение закона Бойля - Мариотта состоит в следующем :
В математической форме это утверждение записывается в виде формулы
p V = C , {\displaystyle pV=C,}где p {\displaystyle p} - давление газа; V {\displaystyle V} - объём газа, а C {\displaystyle C} - постоянная в оговоренных условиях величина. В общем случае значение C {\displaystyle C} определяется химической природой, массой и температурой газа.
Очевидно, что если индексом 1 обозначить величины, относящиеся к начальному состоянию газа, а индексом 2 - к конечному, то приведённую формулу можно записать в виде
p 1 V 1 = p 2 V 2 {\displaystyle p_{1}V_{1}=p_{2}V_{2}} .Из сказанного и приведённых формул следует вид зависимости давления газа от его объёма в изотермическом процессе:
p = C V . {\displaystyle p={\frac {C}{V}}.}Эта зависимость представляет собой другое, эквивалентное первому, выражение содержания закона Бойля - Мариотта. Она означает, что
Давление некоторой массы газа, находящегося при постоянной температуре, обратно пропорционально его объёму.
Тогда связь начального и конечного состояний газа, участвовавшего в изотермическом процессе, можно выразить в виде:
p 1 p 2 = V 2 V 1 . {\displaystyle {\frac {p_{1}}{p_{2}}}={\frac {V_{2}}{V_{1}}}.}Следует отметить, что применимость этой и приведённой выше формулы, связывающей начальные и конечные давления и объёмы газа друг с другом, не ограничивается случаем изотермических процессов. Формулы остаются справедливыми и в тех случаях, когда в ходе процесса температура изменяется, но в результате процесса конечная температура оказывается равной начальной.
Важно уточнить, что данный закон справедлив только в тех случаях, когда рассматриваемый газ можно считать идеальным . В частности, с высокой точностью закон Бойля - Мариотта выполняется применительно к разреженным газам. Если же газ сильно сжат, то наблюдаются существенные отступления от этого закона.
Следствия
Закон Бойля - Мариотта утверждает, что давление газа в изотермическом процессе обратно пропорционально занимаемому газом объёму. Если учесть, что плотность газа также обратно пропорциональна занимаемому им объёму, то мы придём к заключению:
β T = 1 p . {\displaystyle \beta _{T}={\frac {1}{p}}.}При изотермическом процессе давление газа изменяется прямо пропорционально его плотности.
Таким образом, приходим к выводу:
Изотермический коэффициент сжимаемости идеального газа равен обратной величине его давления.
См. также
Примечания
- Петрушевский Ф. Ф. // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). - СПб. , 1890-1907.
Учеными, изучающими термодинамиче-ские системы, было установлено, что из-менение одного макропараметра системы ве-дет к изменению остальных. Например, по-вышение давления внутри резинового шари-ка при его нагревании вызывает увеличение его объема; повышение температуры твердо-го тела ведет к увеличению его размеров и т. п.
Эти зависимости могут быть довольно сложными. Поэтому сначала рассмотрим су-ществующие связи между макропараметра-ми на примере простейших термодинами-ческих систем, например для разреженных газов. Экспериментально установленные для них функциональные зависимости между фи-зическими величинами называют газовыми законами.
Роберт Бойль (1627—1691). Известный английский физик и химик, который исследовал свойства воздуха (масса и упругость воздуха, степень его разре-женности). На опыте показал, что тем-пература кипения воды зависит от дав-ления окружающей среды. Изучал так-же упругость твердых тел, гидростатику, световые и электрические явления, впе-рвые высказал мнение о сложном спек-тре белого света. Ввел понятие «хими-ческий элемент».
Первый газовый закон был открыт анг-лийским ученым Р. Бойлем в 1662 г. при исследовании упругости воздуха. Он взял длинную согнутую стеклянную трубку, за-паянную с одного конца, и начал наливать в нее ртуть до тех пор, пока в коротком колене не образовался небольшой закрытый объем воздуха (рис. 1.5). Затем доливал ртуть в длинное колено, изучая зависимость между объемом воздуха в запаянном конце трубки и давлением, созданным ртутью в левом колене. Предположение ученого о том, что между ними существует опреде-ленная зависимость, подтвердилось. Срав-нивая полученные результаты, Бойль сформу-лировал следующее положение:
между дав-лением и объемом данной массы газа при постоянной температуре существует обратная зависимость: p ~ 1 / V.
 |
| Эдм Мариотт |
Эдм Мариотт (1620—1684) . Француз-ский физик, изучавший свойства жид-костей и газов, столкновения упругих тел, колебания маятника, естественные оптические явления. Установил зави-симость между давлением и объемом газов при постоянной температуре и объяснил на ее основании разные при-менения, в частности, как найти высоту местности по показаниям барометра. До-казал увеличение объема воды при ее замерзании.
Немного позже, в 1676 году француз-ский ученый Э. Мариотт независимо от Р. Бойля обобщенно сформулировал газо-вый закон, который теперь называют законом Бойля-Мариотта. По его утверждению, если при определенной температуре данная масса газа занимает объем V 1 при давлении p 1 , а в другом состоянии при этой же температуре его давление и объем рав-няются p 2 и V 2 , то справедливо соотно-шение:
p 1 / p 2 = V 2 / V 1 или p 1 V 1 = p 2 V 2 .
Закон Бойля-Мариотта : если при постоянной темпе-ратуре происходит термодинамический про-цесс, вследствие которого газ переходит из одного состояния (p 1 и V 1) в другое (p2и V 2), то произведение давления на объем данной массы газа при постоянной температуре яв-ляется постоянным:
pV = const. Материал с сайта
Термодинамический процесс, который про-исходит при постоянной температуре, на-зывается изотермическим (от гр. isos — рав-ный, therme — теплота). Графически на коор-динатной плоскости pV он изображается гиперболой, которая называется изотермой (рис. 1.6). Разным температурам отвечают разные изотермы — чем выше температура, тем выше на координатной плоскости pV находится гипербола (T 2 > T 1). Очевидно, что на координатной плоскости рТ и VT изо-термы изображаются прямыми, перпендику-лярными оси температур.
Закон Бойля-Мариотта устанав-ливает соотношение между дав-лением и объемом газа для изотермических процессов: при постоянной температуре объем V данной массы газа обратно пропорциональный его давлению p .
Согласно закону Бойля - Мариотта , при постоянной температуре объем газа обратно пропорционален давлению.
Это означает, что с ростом давления на газ его объем уменьшается, и наоборот. Для неизменного количества газа закон Бойля - Мариотта можяо также интерпретировать следующим образом: при неизменной температуре произведение давления на объем является величиной постоянной. В виде формулы это выражается так:
Р х V = К, где Р - абсолютное даатение, V - объем; К - константа.
Если Р и V меняются, то Р 1 х V 1 = К и Р 2 х V 2 = К.
Совмещение двух уравнений даст Р 1 х V 1 = Р 2 х V 2 .
Если фиксированное количество газа закачать в жесткую емкость, такую, как баллон акваланга, то, поскольку объем баллона остается неизменным, им и будет определяться давление газа внутри него. Если тем же количеством газа заполнить эластичную емкость, например воздушный шар. он будет расширяться, пока давление газа внутри него не сравняется с давлением окружающей среды. В данном случае давление определяет объем емкости.
Эффект от увеличения давления с глубиной погружения на примере пластиковой бутылки. По мере увеличения давления на газ его объем уменьшается, и наоборот
На уровне моря давление равно 1 бар. На глубине 10 метров давление удваивается до 2 бар и далее с каждыми 10 метрами погружения увеличивается на 1 бар. Представьте перевернутую стеклянную бутылку без пробки, внутри которой находится воздух. При погружении бутылки на глубину 10 метров, где давление составляет 2 бар. воздух внутри нее сожмется до половины своего первоначального объема. На глубине 20 метров давление будет равно 3 бар. а воздух сожмется до трети первоначального объема. На 30 метрах глубины, где давление возрастает до 4 бар. объем воздуха составит лишь четверть от первоначатыюго.
Если давление и объем газа - величины обратно пропорциональные, то давление и плотность прямо пропорциональны. С увеличением давления газа и уменьшением его объема расстояние между молекулами газа сокращается, и газ становится плотнее. При давлении, вдвое превышающем атмосферное, заданный объем газа вдвое плотнее воздуха у поверхности воды и т. д. Поэтому на глубине дайверы быстрее расходуют имеющийся у них запас воздуха. Полный вдох воздуха, давление которого вдвое превышает атмосферное, содержит вдвое больше молекул воздуха, чем воздух на поверхности. Поэтому при давлении в 3 атмосферы баллона хватит лишь на треть того времени, в течение которого человек мог бы пользоваться этим баллоном на поверхности.
Дайвер должен дышать воздухом, давление которого равно давлению окружающей водной среды. Только тогда независимо от глубины погружения будет обеспечиваться расширение воздуха до нормального объема легких. Регулятор воздуха представляет собой систему клапанов, снижающих давление сжатого в баллоне воздуха до давления воды на уровне легких дайвера. Дайверы не хотят понапрасну расходовать воздух в своем баллоне, поэтому регулятор сконструирован так. чтобы подавать воздух только тогда, когда это нужно. Отсюда другое название - «demand valve». то есть клапан, срабатывающий по требованию.
При каждом погружении дайверы несут на себе различные элементы снаряжения, содержащие газ, включая устройства для контроля плавучести, баллоны, маски, «мокрые» и «сухие» неопреновые гидрокостюмы из материала, содержащего его крошечные пузырьки воздуха. В нашем теле также есть наполненные газом полости: пазухи, уши. желудок и легкие. За исключением жестких баллонов, все газонаполненные полости сжимаются при погружении и расширяются при всплытии. При подъеме к поверхности дайверы должны освобождаться от расширяющегося в легких воздуха, выравнивать давление в ушах и пазухах во избежание боли и повреждения тканей, именуемого баротравмой. (Это не касается декомпрессионных остановок - о них разговор особый.)
Считается, что расширение газов в организме дайвера идет особенно интенсивно на последних 10 метрах подъема, вот почему на этом этапе подниматься следует медленно, постепенно выдыхая воздух.
Состав морской воды
Среди химических соединений, придающих морской воде ее соленый вкус, преобладает поваренная соль (хлорид натрия). В среднем в морской воде содержится примерно 3% соли, хотя этот показатель может варьироваться от 1% в полярных морях до 5% в замкнутых, таких, как Средиземное и Красное. Соль, получаемая при выпаривании морской воды, на 77,76% состоит из хлорида натрия, на 10,88% - из хлорида магния, на 4,74% - из сульфата магния, на 3,60% - из сульфата кальция, на 2,46% - из хлорида калия, на 0,22% - из бромида магния и на 0,34% из карбоната кальция.