Каждому известно, что вода может находиться в природе в трех агрегатных состояниях - твердом, жидком и газообразном. При плавлении происходит превращение твердого льда в жидкость, а при дальнейшем нагревании жидкость испаряется, образуя водяной пар. Каковы же условия плавления, кристаллизации, испарения и конденсации воды? При какой температуре тает лед или образуется пар? Об этом мы поговорим в данной статье.
Нельзя сказать, что водяной пар и лед редко встречаются в повседневной жизни. Однако наиболее распространенным является именно жидкое состояние - обычная вода. Специалисты выяснили, что на нашей планете находится более 1 млрд кубических километров воды. Однако не более 3 млн км 3 воды принадлежат пресным водоемам. Достаточно большое количество пресной воды «покоится» в ледниках (около 30 млн кубических километров). Однако растопить лед таких огромных глыб далеко не просто. Остальная же вода соленая, принадлежащая морям Мирового океана.
Вода окружает современного человека повсюду, во время большинства ежедневных процедур. Многие считают, что запасы воды неиссякаемы, и человечество сможет всегда использовать ресурсы гидросферы Земли. Однако это далеко не так. Водные ресурсы нашей планеты постепенно истощаются, и уже через несколько сотен лет пресной воды на Земле может не остаться вовсе. Поэтому абсолютно каждому человеку нужно бережно относиться к пресной воде и экономить ее. Ведь даже в наше время существуют государства, в которых запасы воды катастрофически малы.
Свойства воды

Прежде чем говорить о температуре таяния льда, стоит рассмотреть основные свойства этой уникальной жидкости.
Итак, воде присущи следующие свойства:
- Отсутствие цвета.
- Отсутствие запаха.
- Отсутствие вкуса (однако качественная питьевая вода имеет приятный вкус).
- Прозрачность.
- Текучесть.
- Способность растворять различные вещества (например, соли, щелочи и т. д.).
- Вода не имеет собственной постоянной формы и способна принимать форму сосуда, в который попадает.
- Способность очищаться посредством фильтрования.
- При нагревании вода расширяется, а при охлаждении сжимается.
- Вода может испаряться, превращаясь в пар, и замерзать, образуя кристаллический лед.
В этом списке представлены основные свойства воды. Теперь разберемся, каковы особенности твердого агрегатного состояния этого вещества, и при какой температуре тает лед.

Лед - это твердое кристаллическое вещество, которое имеет достаточно неустойчивую структуру. Он, как и вода, прозрачен, не имеет цвета и запаха. Также лед обладает такими свойствами, как хрупкость и скользкость; он холодный на ощупь.
Снег также представляет собой замерзшую воду, однако обладает рыхлой структурой и имеет белый цвет. Именно снег каждый год выпадает в большинстве стран мира.
Как снег, так и лед - крайне неустойчивые вещества. Чтобы растопить лед, не нужно прикладывать особых усилий. Когда же он начинает таять?

В природе твердый лед существует только при температуре 0 °C и ниже. Если же температура окружающей среды поднимается и становится больше 0 °C, лед начинает таять.
При температуре таяния льда, при 0 °C, происходит и другой процесс - замерзание, или кристаллизация, жидкой воды.
Данный процесс можно наблюдать всем жителям умеренно континентального климата. Зимой, когда температура на улице опускается ниже 0 °C, достаточно часто выпадает снег, который не тает. А жидкая вода, находившаяся на улицах, замерзает, превращаясь в твердый снег или лед. Весной же можно увидеть обратный процесс. Температура окружающей среды поднимается, поэтому лед и снег тают, образуя многочисленные лужи и грязь, которую можно считать единственным минусом весеннего потепления.
Таким образом, можно сделать вывод, что, при какой температуре начинает таять лед, при такой же температуре начинается и процесс замерзания воды.
Количество теплоты

В такой науке, как физика, часто используется понятие количества теплоты. Данная величина показывает количество энергии, необходимой для нагревания, плавления, кристаллизации, кипения, испарения или конденсации различных веществ. Причем каждый из перечисленных процессов имеет свои особенности. Поговорим о том, какое количество теплоты для нагревания льда требуется в обычных условиях.
Чтобы нагреть лед, нужно сначала его растопить. Для этого необходимо количество теплоты, нужное для плавления твердого вещества. Теплота равняется произведению массы льда на удельную теплоту его плавления (330-345 тысяч Джоулей/кг) и выражается в Джоулях. Допустим, что нам дано 2 кг твердого льда. Таким образом, чтобы его растопить, нам понадобится: 2 кг * 340 кДж/кг = 680 кДж.
После этого нам необходимо нагреть образовавшуюся воду. Количество теплоты для данного процесса рассчитать будет немного сложнее. Для этого нужно знать начальную и конечную температуру нагреваемой воды.
Итак, допустим, что нам требуется нагреть получившуюся в результате плавления льда воду на 50 °C. То есть разница начальной и конечной температуры = 50 °C (начальная температура воды - 0 °C). Тогда следует умножить разность температур на массу воды и на ее удельную теплоемкость, которая равняется 4 200 Дж*кг/°C. То есть количество теплоты, необходимое для нагревания воды, = 2 кг * 50 °C * 4 200 Дж*кг/°C = 420 кДж.
Тогда получаем, что для плавления льда и последующего нагревания получившейся воды нам потребуется: 680 000 Дж + 420 000 Дж = 1 100 000 Джоулей, или 1,1 Мегаджоуль.
Зная, при какой температуре тает лед, можно решить множество непростых задач по физике или химии.
В заключение
Итак, в данной статье мы узнали некоторые факты о воде и о двух ее агрегатных состояниях - твердом и жидком. Водяной пар, однако, представляет собой не менее интересный объект для изучения. Например, в нашей атмосфере содержится приблизительно 25*10 16 кубических метров водяного пара. К тому же, в отличие от замерзания, испарение воды происходит при любой температуре и ускоряется при ее нагревании или при наличии ветра.
Мы узнали, при какой температуре тает лед и замерзает жидкая вода. Такие факты всегда пригодятся нам в повседневной жизни, так как вода окружает нас повсюду. Важно всегда помнить о том, что вода, в особенности пресная, является иссякаемым ресурсом Земли и нуждается в бережном к ней отношении.
Для того, чтобы расплавить какое-либо вещество в твердом состоянии, необходимо его нагреть. И при нагревании любого тела отмечается одна любопытная особенность
Особенность такая: температура тела растет вплоть до температуры плавления, а потом останавливается до того момента, пока все тело целиком не перейдет в жидкое состояние. После расплавления температура вновь начинает расти, если, конечно, продолжать нагревание. То есть, существует промежуток времени, во время которого мы нагреваем тело, а оно не нагревается. Куда же девается энергия тепла, которую мы расходуем? Чтобы ответить на этот вопрос, надо заглянуть внутрь тела.
В твердом теле молекулы расположены в определенном порядке в виде кристаллов. Они практически не двигаются, лишь слегка колеблясь на месте. Для того, чтобы вещество перешло в жидкое состояние, молекулам необходимо придать дополнительную энергию, чтобы они смогли вырваться от притяжения соседних молекул в кристалликах. Нагревая тело, мы придаем молекулам эту необходимую энергию. И вот пока все молекулы не получат достаточно энергии и не разрушатся все кристаллики, температура тела не повышается. Опыты показывают, что для разных веществ одной массы требуется разное количество теплоты для полного его расплавления.
То есть существует определенная величина, от которой зависит, сколько тепла необходимо поглотить веществу для расплавления . И величина эта различна для разных веществ. Эта величина в физике называется удельная теплота плавления вещества. Опять же, вследствие опытов установлены значения удельной теплота плавления для различных веществ и собраны в специальные таблицы, из которых можно почерпнуть эти сведения. Обозначают удельную теплоту плавления греческой буквой λ (лямбда), а единицей измерения является 1 Дж/кг.
Формула удельной теплоты плавления
Удельная теплота плавления находится по формуле:
где Q - это количество теплоты, необходимое для того, чтобы расплавить тело массой m.
Опять-таки из опытов известно, что при отвердевании вещества выделяют такое же количество тепла, которое требовалось затратить на их расплавление. Молекулы, теряя энергию, образуют кристаллы, будучи не в силах сопротивляться притяжению других молекул. И опять-таки, температура тела не будет понижаться вплоть до того момента, пока не отвердеет все тело, и пока не выделится вся энергия, которая была затрачена на его плавление. То есть удельная теплота плавления показывает, как сколько надо затратить энергии, чтобы расплавить тело массой m, так и сколько энергии выделится при отвердевании данного тела.
Для примера, удельная теплота плавления воды в твердом состоянии, то есть, удельная теплота плавления льда равна 3,4*105 Дж/кг. Эти данные позволяют рассчитать, сколько потребуется энергии, чтобы расплавить лед любой массы. Зная также удельную теплоемкость льда и воды, можно рассчитать, сколько точно потребуется энергии для конкретного процесса, например, расплавить лед массой 2 кг и температурой - 30˚С и довести получившуюся воду до кипения. Такие сведения для различных веществ очень нужны в промышленности для расчета реальных затрат энергии при производстве каких-либо товаров.
Плавление
Плавление — это процесс превращения вещества из твёрдого состояния в жидкое.
Наблюдения показывают, что если измельчённый лёд, имеющий, например, температуру 10 °С, оставить в тёплой комнате, то его температура будет повышаться. При 0 °С лёд начнет таять, а температура при этом не будет изменяться до тех пор, пока весь лёд не превратится в жидкость. После этого температура образовавшейся изо льда воды будет повышаться.
Это означает, что кристаллические тела, к которым относится и лед, плавятся при определённой температуре, которую называют температурой плавления . Важно, что во время процесса плавления температура кристаллического вещества и образовавшейся в процессе его плавления жидкости остаётся неизменной.
В описанном выше опыте лёд получал некоторое количество теплоты, его внутренняя энергия увеличивалась за счёт увеличения средней кинетической энергии движения молекул. Затем лёд плавился, его температура при этом не менялась, хотя лёд получал некоторое количество теплоты. Следовательно, его внутренняя энергия увеличивалась, но не за счёт кинетической, а за счёт потенциальной энергии взаимодействия молекул. Получаемая извне энергия расходуется на разрушение кристаллической решетки. Подобным образом происходит плавление любого кристаллического тела.
Аморфные тела не имеют определённой температуры плавления. При повышении температуры они постепенно размягчаются, пока не превратятся в жидкость.
Кристаллизация
Кристаллизация — это процесс перехода вещества из жидкого состояния в твёрдое состояние. Охлаждаясь, жидкость будет отдавать некоторое количество теплоты окружающему воздуху. При этом будет уменьшаться её внутренняя энергия за счёт уменьшения средней кинетической энергии его молекул. При определённой температуре начнётся процесс кристаллизации, во время этого процесса температура вещества не будет изменяться, пока всё вещество не перейдет в твёрдое состояние. Этот переход сопровождается выделением определённого количества теплоты и соответственно уменьшением внутренней энергии вещества за счёт уменьшения потенциальной энергии взаимодействия его молекул.
Таким образом, переход вещества из жидкого состояния в твёрдое состояние происходит при определённой температуре, называемой температурой кристаллизации. Эта температура остаётся неизменной в течение всего процесса плавления. Она равна температуре плавления этого вещества.
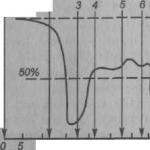
На рисунке приведён график зависимости температуры твёрдого кристаллического вещества от времени в процессе его нагревания от комнатной температуры до температуры плавления, плавления, нагревания вещества в жидком состоянии, охлаждения жидкого вещества, кристаллизации и последующего охлаждения вещества в твёрдом состоянии.
Удельная теплота плавления
Различные кристаллические вещества имеют разное строение. Соответственно, для того, чтобы разрушить кристаллическую решётку твёрдого тела при температуре его плавления, необходимо ему сообщить разное количество теплоты.
Удельная теплота плавления — это количество теплоты, которое необходимо сообщить 1 кг кристаллического вещества, чтобы превратить его в жидкость при температуре плавления. Опыт показывает, что удельная теплота плавления равна удельной теплоте кристаллизации .
Удельная теплота плавления обозначается буквой λ . Единица удельной теплоты плавления — [λ] = 1 Дж/кг .
Значения удельной теплоты плавления кристаллических веществ приведены в таблице. Удельная теплота плавления алюминия 3,9*10 5 Дж/кг. Это означает, что для плавления 1 кг алюминия при температуре плавления необходимо затратить количество теплоты 3,9*10 5 Дж. Этому же значению равно увеличение внутренней энергии 1 кг алюминия.
Чтобы вычислить количество теплоты Q , необходимое для плавления вещества массой m , взятого при температуре плавления, следует удельную теплоту плавления λ умножить на массу вещества: Q = λm .
Эта же формула используется при вычислении количества теплоты, выделяющегося при кристаллизации жидкости.

Конспект урока «Плавление и кристаллизация. Удельная теплота плавления».
Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты. Количество теплоты зависит от массы тела, от разности температур тела и от рода вещества.
[Q]=Дж или калориях
1 кал – это количество теплоты, которое необходимо для нагревания 1 г воды на 1 о С.
Удельная теплоемкость – физическая величина, равная количеству теплоты, которое необходимо передать телу массой 1 кг для того, чтобы его температура изменилась на 1 о С.
[C] = Дж/кг о С
Удельная теплоемкость воды 4200 Дж/кг о С. Это значит, что для нагревания воды массой 1 кг на 1 о С необходимо затратить 4200 Дж теплоты.
Удельная теплоемкость вещества, находящегося в различных агрегатных состояниях, различна. Так, теплоемкость льда 2100 Дж/кг о С. Удельная теплоемкость воды самая большая. В связи с этим вода в морях и океанах, нагреваясь летом, поглощает большое количество теплоты. Зимой вода остывает и отдает большое количество теплоты. Поэтому в районах, расположенных вблизи водоемов, летом не бывает очень жарко, а зимой очень холодно. Из-за высокой теплоемкости воду широко применяют в технике и быту. Например, в отопительных системах домов, при охлаждении деталей во время их обработки на станках, медицине (грелках) и т.д.
С возрастанием температуры твердых тел и жидкостей возрастает кинетическая энергия их частиц: они начинают колебаться с большей скоростью. При некоторой температуре, вполне определенной для данного вещества, силы притяжения между частицами уже не в состоянии удержать их в узлах кристаллической решетки (дальний порядок превращается в ближний), и кристалл начинает плавиться, т.е. вещество начинает переходить в жидкое состояние.
Плавление – процесс перехода вещества из твердого состояния в жидкое.
Отвердевание (кристаллизация) – процесс перехода вещества из жидкого состояния в твердое.
 В процессе плавления температура кристалла остается постоянной. Эта температура называется температурой плавления
. У каждого вещества есть своя температура плавления. Находят по таблице.
В процессе плавления температура кристалла остается постоянной. Эта температура называется температурой плавления
. У каждого вещества есть своя температура плавления. Находят по таблице.
Постоянство температуры при плавлении имеет большое практическое значение, поскольку позволяет градуировать термометры, изготавливать плавкие предохранители и индикаторы, которые расплавляются при строго заданной температуре. Знание температуры плавления различных веществ важно и с чисто бытовой точки зрения: в противном случае кто поручится за то, что эта кастрюля или сковородка не расплавится на огне газовой горелки?
Температура плавления и равная ей температура отвердевания - характерный признак вещества. Ртуть плавится и затвердевает при температуре -39 о С, поэтому в районах Крайнего Севера ртутные термометры не используют. Вместо ртутных термометров в этих широтах используют спиртовые (-114 о С). Самым тугоплавким металлом является вольфрам (3420 о С).
Количество теплоты, необходимое для плавления вещества, определяют по формуле:
Где m – масса вещества, - удельная теплота плавления.
Дж/кг
Удельная теплота плавления – такое количество теплоты, которое необходимо для расплавления 1 кг вещества, взятого при температуре плавления. У каждого вещества своя. Её находят по таблице.
Температура плавления вещества зависит от давления. Для веществ, у которых объем при плавлении возрастает, повышение давления повышает температуру плавления и наоборот. У воды объем при плавлении уменьшается, и при повышении давления лед плавится при более низкой температуре.
Билет № 14
Переход вещества из твердого кристаллического состояния в жидкое называется плавлением . Чтобы расплавить твердое кристаллическое тело, его нужно нагреть до определенной температуры, т. е. подвести тепло. Температура, при которой вещество плавится, называется температурой плавления вещества.
Обратный процесс — переход из жидкого состояния в твердое — происходит при понижении температуры, т. е. тепло отводится. Переход вещества из жидкого состояния в твердое называется отвердеванием, или кристал лизацией. Температура, при которой вещество кристаллизуется, называется температурой кристалли зации.
Опыт показывает, что любое вещество кристаллизуется и плавится при одной и той же температуре.
На рисунке представлен график зависимости температуры кристаллического тела (льда) от времени нагревания (от точки А до точки D) и времени охлаждения (от точки D до точки K ). На нем по горизонтальной оси отложено время, а по вертикальной — температура.
Из графика видно, что наблюдение за процессом началось с момента, когда температура льда была -40 °С, или, как принято говорить, температура в начальный момент времени t нач = -40 °С (точка А на графике). При дальнейшем нагревании температура льда растет (на графике это участок АВ ). Увеличение температуры происходит до 0 °С — температуры плавления льда. При 0°С лед начинает плавиться, а его температура перестает расти. В течение всего времени плавления (т.е. пока весь лед не расплавится) температура льда не меняется, хотя горелка продолжает го-реть и тепло, следовательно, подводится. Процессу плавления соответствует горизонтальный учас-ток графика ВС. Только после того как весь лед расплавится и превратится в воду , температура снова начинает подниматься (участок CD ). После того, как температура воды достигнет +40 °С, горелку гасят и воду начинают охлаждать, т. е. тепло отводят (для этого можно сосуд с водой по-местить в другой, больший сосуд со льдом). Температура воды начинает снижаться (участок DE ). При достижении температуры 0 °С температура воды перестает снижаться, несмотря на то, что тепло по-прежнему отводится. Это идет процесс кристаллизации воды — образования льда (гори-зонтальный участок EF ). Пока вся вода не превратится в лед, температура не изменится. Лишь после этого начинает уменьшаться температура льда (участок FK ).
Вид рассмотренного графика объясняется следующим образом. На участке АВ благодаря подводимому теплу средняя кинетическая энергия молекул льда увеличивается, и температура его повышается. На участке ВС вся энергия, получаемая содержимым колбы, тратится на разрушение кристаллической решетки льда: упорядоченное пространственное расположение его молекул сменяется неупорядоченным, меняется расстояние между молекулами, т.е. происходит перестройка молекул таким образом, что вещество становится жидким. Средняя кинетическая энергия моле-кул при этом не меняется, поэтому неизменной остается и температура. Дальнейшее увеличение температуры расплавленного льда-воды (на участке CD ) означает увеличение кинетической энер-гии молекул воды вследствие подводимого горелкой тепла.
При охлаждении воды (участок DE ) часть энергии у нее отбирается, молекулы воды движутся с меньшими скоростями, их средняя кинетическая энергия падает — температура уменьшается, вода охлаждается. При 0°С (горизонтальный участок EF ) молекулы начинают выстраиваться в определенном порядке, образуя кристаллическую решетку. Пока этот процесс не завершится, температура вещества не изменится, несмотря на отводимое тепло, а это означает, что при отвер-девании жидкость (вода) выделяет энергию. Это как раз та энергия, которую поглотил лед, пре-вращаясь в жидкость (участок ВС ). Внутренняя энергия у жидкости больше, чем у твердого тела. При плавлении (и кристаллизации) внутренняя энергия тела меняется скачком.
Металлы, плавящиеся при температуре выше 1650 ºС, называют тугоплавкими (титан, хром , молибден и др.). Самая высокая температура плавления среди них у вольфрама — около 3400 °С . Тугоплавкие металлы и их соединения используют в качестве жаропрочных материалов в самолетостроении, ракетостроении и космической технике, атомной энергетике.
Подчеркнем еще раз, что при плавлении вещество поглощает энергию. При кристаллизации оно, наоборот, отдает ее в окружающую среду. Получая определенное количество теплоты, выделяющееся при кристаллизации, среда нагревается. Это хорошо известно многим птицам. Неда-ром их можно заметить зимой в морозную погоду сидящими на льду, который покрывает реки и озера. Из-за выделения энергии при образовании льда воздух над ним оказывается на несколько градусов теплее, чем в лесу на деревьях, и птицы этим пользуются.
Плавление аморфных веществ.
Наличие определенной точки плавления — это важный признак кристаллических веществ. Именно по этому признаку их можно легко отличить от аморфных тел, которые также относят к твердым телам. К ним, в частности, относятся стекла, очень вязкие смолы, пластмассы.
Аморфные вещества (в отличие от кристаллических) не имеют определенной температуры плавления — они не плавятся, а размягчаются. При нагревании кусок стекла, например, снача-ла становится из твердого мягким, его легко можно гнуть или растягивать; при более высокой температуре кусок начинает менять свою форму под действием собственной тяжести. По мере нагревания густая вязкая масса принимает форму того сосуда, в котором лежит. Эта масса сначала густая, как мед, затем — как сметана и, наконец, становится почти такой же маловязкой жидкостью, как вода. Однако указать определенную температуру перехода твердого тела в жидкое здесь невозможно, поскольку ее нет.
Причины этого лежат в коренном отличии строения аморфных тел от строения кристаллических. Атомы в аморфных телах расположены беспорядочно. Аморфные тела по своему строению напоминают жидкости. Уже в твердом стекле атомы расположены беспорядочно. Значит, повы-шение температуры стекла лишь увеличивает размах колебаний его молекул, дает им постепенно все большую и большую свободу перемещения. Поэтому стекло размягчается постепенно и не обнаруживает резкого перехода «твердое—жидкое», характерного для перехода от расположения молекул в строгом порядке к беспорядочному.
Теплота плавления.
Теплота плавления — это количество теплоты, которое необходимо сообщить веществу при постоянном давлении и постоянной температуре, равной температуре плавления, чтобы полностью перевести его из твердого кристаллического состояния в жидкое. Теплота плавления равна тому количеству теплоты , которое выделяется при кристалли-зации вещества из жидкого состояния. При плавлении вся подводимая к веществу теплота идет на увеличение потенциальной энер-гии его молекул. Кинетическая энергия не меняется, поскольку плавление идет при постоянной температуре.
Изучая на опыте плавление различных веществ одной и той же массы, можно заметить, что для превращения их в жидкость требуется разное количество теплоты. Например, для того чтобы расплавить один килограмм льда, нужно затратить 332 Дж энергии, а для того чтобы расплавить 1 кг свинца — 25 кДж .
Количество теплоты, выделяемое телом, считается отрицательным. Поэтому при расчете количества теплоты, выделяющегося при кристаллизации вещества массой m , следует пользоваться той же формулой, но со знаком «минус»:
Теплота сгорания.
Теплота сгорания (или теплотворная способность , калорийность ) — это количество теплоты, выделяющейся при полном сгорании топлива.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива. Обыч-ное топливо (уголь, нефть, бензин) содержит углерод . При горении атомы углерода соединяются с атомами кислорода , содержащегося в воздухе, в результате чего образуются молекулы углекислого газа . Кинетическая энергия этих молекул оказывается большей, чем у исходных частиц. Увеличение кинетической энергии молекул в процессе горения называют выделением энергии. Энергия, выделяющаяся при полном сгорании топлива, и есть теплота сгорания этого топлива.
Теплота сгорания топлива зависит от вида топлива и его массы. Чем больше масса топлива, тем больше количество теплоты, выделяющейся при его полном сгорании.
Физическая величина , показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива. Удельную теплоту сгорания обозначают буквой q и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты Q , выделяющееся при сгорании m кг топлива, определяют по формуле:
Чтобы найти количество теплоты, выделяющееся при полном сгорании топлива произвольной массы, нужно удельную теплоту сгорания этого топлива умножить на его массу.