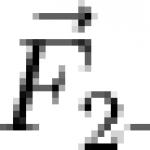В справочната таблица, освен поредния номер на елементите, техния символ, наименование и атомно тегло, е дадена и кратка информация. историческа информация: кой и кога е открил този или онзи елемент. Датите, посочени в таблицата, съответстват предимно на онези години, когато елементите са получени в чиста форма, тоест в метално или свободно състояние, а не във формата химични съединения; Посочено е и името на учения, който първи е постигнал това. Допълнителни насоки по тези въпроси са предоставени за някои елементи в бележките към таблицата. В таблицата е въведено съкращението “Изв.” с други." означава „известен от древни времена“, останалите съкращения са ясни.
|
Атомен номер Z |
Име |
Атомно тегло А |
Кой отвори |
Година на откриване на елемента |
|
|
Кавендиш |
|||||
|
Рамзи и Клив |
|||||
|
Арфведсон |
|||||
|
Берилий |
Велер и Бюси |
||||
|
Гей-Люсак и Тенар |
|||||
|
Изв. с други |
|||||
|
Д. Ръдърфорд |
|||||
|
Кислород |
Пристли и Шеле |
||||
|
Рамзи и Травърс |
|||||
|
Либих и Бюси |
|||||
|
Алуминий |
|||||
|
Берцелиус |
|||||
|
Изв. с други |
|||||
|
Рейли и Рамзи |
|||||
|
Деви (Берцелиус) |
|||||
|
Зефстрьом |
|||||
|
Манган |
|||||
|
Изв. с други |
|||||
|
Кронщед |
|||||
|
Изв. с други |
|||||
|
маркграф |
|||||
|
Лекок дьо Боабодран |
|||||
|
Германий |
|||||
|
Алберт Велики |
|||||
|
Берцелиус |
|||||
|
Рамзи и Травърс |
|||||
|
Бунзен и Кирхоф |
|||||
|
Стронций |
|||||
|
Цирконий |
Берцелиус |
||||
|
Молибден |
|||||
|
Технеций |
Перие и Сегре |
||||
|
Уоластън |
|||||
|
Паладий |
Уоластън |
||||
|
Изв. с други |
|||||
|
Херман и Стромберг |
|||||
|
Райх и Рихтер |
|||||
|
Изв. с други |
|||||
|
В. Валентин |
|||||
|
Рихенщайн |
|||||
|
Рамзи и Травърс |
|||||
|
Бунзен и Кирхоф |
|||||
|
Мозандер |
|||||
|
Халдербранд и Нортън |
|||||
|
Празеодим |
|||||
|
Прометий |
Марянски и Гленденев |
||||
|
Лекок дьо Боабодран |
|||||
|
Демарсей |
|||||
|
Гадолиний |
Мариняк и Лекок дьо Боабодран |
||||
|
Мозандер |
|||||
|
Диспрозий |
Лекок дьо Боабодран |
||||
|
Мозандер |
|||||
|
Итербий |
Мариняк |
||||
|
Огън и Хевеси |
|||||
|
Волфрам |
бр. д'Елюар |
||||
|
Нодак и Таске |
|||||
|
платина 9) |
Споменаване през 16 век |
||||
|
Изв. с други |
|||||
|
Споменаване за 3 век пр.н.е V. |
|||||
|
Споменаване Плиний |
|||||
|
Споменаване В. Валентин през 15 век. |
|||||
|
Корзон и Макензи |
|||||
|
Берцелиус |
|||||
|
Протактиний |
Майтнер и Хан |
||||
|
Нептуний |
Макмилън и Абелсън |
||||
|
Плутоний |
Сиборг и Макмилан |
||||
|
америций |
Сиборг и Джеймс |
||||
|
Сиборг и Джеймс |
|||||
|
беркелий |
Сиборг и Томпсън |
||||
|
Калифорния |
Сиборг и Томпсън |
||||
|
Айнщайний |
|||||
|
Менделевий |
Бележки на масата:
1) Янсен и, независимо от него, Локиър през 1868 г. откриват неизвестни преди това линии в спектъра на слънцето; този нов елемент беше наречен хелий, защото се смяташе, че се намира само в слънцето. 27 години по-късно Рамзи и Клив откриват същите линии в спектъра на нов газ, получен от анализа на минерала клевеит; името хелий за този елемент беше запазено.
2) Обратно в края на 18 век. Известно е, че когато сярната киселина действа върху флуорипат, се отделя специална киселина, която разяжда стъклото. През 1810 г. Ампер показва, че тази киселина е подобна на солната киселина и е съединение с водород на някакъв неизвестен елемент, който той нарича флуор. Moissan успя да получи флуор в чиста форма едва през 1886 г.
3) Магнезиевият оксид е известен отдавна, той е изследван от Блек през 1775 г. Деви се опита да получи метален магнезий през 1808 г., но не успя да получи метала в чистата му форма.
4) Титановият диоксид е получен в лабораторията в края на 18 век; Берцелиус получава титан, но не напълно чист. По-чист метален титан е получен от Грегор, след това от Мойсан.
5) Съединенията на арсенова сяра са били известни в древността.
6) В началото на 19в. получена е смес от ниобий и тантал, която се счита за нов елемент; е дадено името Колумбия. В Америка и Англия ниобият все още се нарича колумбий.
7) Церият е получен под формата на оксид през 1803 г.
8) Дълго време сместа от празеодим и неодим се счита за отделен елемент, който се нарича дидий (Di).
9) Платината е описана като специален метал през 1750 г.; преди 1810 г. единственото място, където се добиваше платина, беше Колумбия. След това платината е открита на други места, включително Урал, който все още е най-богатият източник на нейното производство.
10) Урановият диоксид, получен за първи път през 1789 г., първоначално е погрешно смятан за нов елемент. Металният уран е получен за първи път през 1842 г., неговите радиоактивни свойства са открити едва през 1896 г.
_______________
Източник на информация:КРАТКО ФИЗИКО-ТЕХНИЧЕСКО РЪКОВОДСТВО / Том 1, - М.: 1960.
Как и кога са открити първите химикали? Историята на откриването на елементите датира от древни времена. Когато човекът за първи път откри огъня, той започна да оставя въглищата, образувани от изгарянето на дърва, в горите. Моят първи " произведение на изкуството„Човекът направи и парче въглен на стената на пещерата.
История на откриването на химичните елементи
През каменната ера от камък са били издълбани инструменти и оръжия: върхове на копия, чукове и ножове. Жители древна индияпостигнали забележителни резултати в изкуството на обработката естествени материали. Техните съдове са направени от глина, тоест от съединения на алуминий, силиций и кислород.
Откриване на първите метали
Разбира се, по това време никой не е имал представа, че съществуват химически елементи или че глината и камъкът се състоят от някакви отделни части. С течение на времето човекът започна да овладява това, което го заобикаляше; той започна да извлича елементи от материалите, които намираше в земята, и да ги обработва. Сега наричаме тази руда „богата земя“.
Галенитът или оловният сулфид е доста широко разпространена руда. И древните хора са получавали олово от галенит чрез процес, който по същество е открит случайно. От оловна руда, смесена с въглища, на огъня се отделяха капчици чисто метално олово.
Друга известна руда древен човек, беше цинобър или живачен сулфид. Когато тази руда се нагрее, химическа реакция, което води до образуването на чист живак.
Любопитството на човека и способността му да обработва материали постепенно нарастват; той откри самородната мед и се научи да извлича мед и калай от техните руди. Чрез смесване на мед и калай той получи бронз. Това бележи толкова важен етап в човешката история, че го наричаме Бронзовата епоха.
През този период се изработват чудесни инструменти и оръжия, както и изключително фини бижута. Тук възниква металургията като наука.
Желязната епоха започва хиляда години пр. н. е. с откриването на топенето на желязо. Всъщност желязото очевидно е било откривано и преоткривано много пъти преди това време. За първи път е открит в пепелта от големи пожари близо до скали, съдържащи червена руда.
От желязо са правени чукове, шила, ключове, гребени и, разбира се, оръжия. В онези дни възходът и падението на цивилизацията са пряко свързани със степента на развитие на металургията, с уменията на занаятчиите от различни нации.
Основното е, че човек се е научил да извлича елементи от заобикалящата го природа, от руди, съдържащи тези елементи. Първоначалният метод беше много груб и включваше използването на топлина и, в някои случаи, въглища. Изисква само огън за изпълнение и, разбира се, лесно се възпроизвежда в лаборатория.
Нека поставим парче руда, например олово, върху графитна плоча и да я нагреем. Резултатът е сравнително чисто парче олово.
Веднъж извлечено от неговите руди или открито в чиста форма, какъвто беше случаят със златото, примитивен човекТой бързо откри, че металът може да бъде оформен в различни форми. Той се научи да кове метал и дори да прави тънки като лист плочи.
Тогава първобитният човек се е научил да борави с някои други химически елементи, въпреки че, разбира се, не е знаел и не е подозирал, че има работа с елементи.
Естествено, той придоби въглерод под формата на въглища. Той също така познаваше сярата и елементите, които се срещат в природата в естествено състояние: злато, сребро и мед. Той се научи да извлича чисти метали - мед, живак, олово и калай - от рудите.
Но очевидно основното постижение на човека е способността му да получава метално желязо от руди. Разпространението на желязото сред някои народи определя до известна степен местоположението на центровете на цивилизацията в зората на металургията.
пр.н.е. тези девет химически елементии са били известни на човека, те са били добивани и използвани съвсем съзнателно. Ако тези елементи се поставят в съвременната периодична таблица, тогава някои от тях ще се окажат много сходни по своите химични свойства.
Медта, среброто и златото имат подобни свойства. Същото важи и за калая и оловото. Химическите символи за тези девет елемента са:
- C (въглерод)
- Si (мед)
- Ai (злато)
- S (сяра)
- Ag (сребро)
- Hg (живак)
- Fe (желязо)
- Sn (калай)
- Pb (олово)
История на откриването на химичните елементи през Средновековието
Нищо съществено не е направено в областта на откриването на химични елементи до периода, наречен Средновековие. По това време се появяват алхимиците. Те са работили с примитивни съоръжения - реторти, хавани и пестици, които сега имат само символично значение за нас.
Алхимиците провеждат различни експерименти, вариращи от тези, които се отнасят до областта на магията (например търсенето на еликсира на живота), до експерименти, предшестващи съвременната химия.
Алхимиците често говореха за "философски камък", с който се надяваха да превърнат обикновените метали в злато. Сега е трудно да се каже какво са взели за това митично вещество. Може би не беше конкретно нещо или дори камък. Някои историци смятат, че това е живачен сулфид, но други са на друго мнение.
Освен тези напразни опити, алхимиците са първите, които извършват редица важни химични експерименти. Те, например, извличаха метали от руди, въпреки че това не беше необичайно в сравнение с предишните постижения на металургията.
Откриване на киселини
Тяхното най-важно творение са киселините, които много по-късно стават основните продукти на индустриалната химия.
Един от техните експерименти включваше нагряване на вещество, подобно на железен сулфат, и освобождаване на това, което те нарекоха витриол. Това съединение сега е известно като сярна киселина.
Алхимиците също знаеха как да произвеждат солна и азотна киселина и произвеждаха други химикали: поташ и натриев карбонат, които по-късно се оказаха важни индустриални продукти.
Въпреки техните донякъде чужди методи и цели, алхимиците заслужават признание, защото се интересуват както от теория, така и от практически изследвания. Те се опитаха да систематизират знанията, които натрупаха чрез експерименти, с помощта на бележки и скици на своите преживявания. Те вярваха, че елементарните субстанции на природата са огън, и се стремяха да установят логически връзки между тези четири „елемента“. В известен смисъл тяхната странна схема е предшественик на нашата съвременна периодична система.
Откриване на арсен, антимон и бисмут
Несъмнено алхимиците са имали голямо влияние върху развитието на химията. Те направиха много открития и през XII-XIV век успяха да открият три важни химични елемента: арсен (As), антимон (Sb) и бисмут (Bi). Всички те принадлежат към едно и също химическо „семейство“ и са разположени в една и съща вертикална колона на нашата съвременна периодична таблица.
Приликите между тези три елемента показват, че груб химични методиалхимиците вероятно са били ограничени до един конкретен тип експеримент, в който химичните свойства от определен тип играят важна роля.
След това трио (арсен, антимон, бисмут) не са открити нови елементи в продължение на няколко века, с изключение на платината, която е изолирана в Мексико около средата на 16 век. Името му идва от испанска дума, която означава „малко сребро“.
През 18-ти век платината очевидно е била използвана само за фалшифициране на златни монети. В продължение на няколко години в началото на 19 век Русия сече платинени монети.
От тринадесетте елемента, известни до средата на 17 век, не знаем кога или от кого е открит. Същото може да се каже и за цинка, който е изолиран в чиста форма в края на 17 век или може би малко по-рано.
Но по това време науката започна да приема доста модерна форма. Хората започнаха да изучават природата, химията и елементите в името на знанията, които могат да бъдат извлечени от техните изследвания. Новите открития бяха записани и публикувани.
Вярно е, че учените от Древна Гърция се интересуват от науката заради самата нея. Те дори създадоха добре развита атомна теория, която е подобна в много отношения на съвременната атомна теория. Гръцките учени обаче не обичали да провеждат експерименти и затова техните теории останали на хартия и никога не били развити.
Откриване на фосфора
Първият химичен елемент, открит от един човек и който наистина може да се счита за негово дете, е фосфорът, което означава „носител на светлина“.
Фосфорът е открит от алхимик и търговец на име Хениг Бранд по време на търсенето му на „философския камък“ в Хамбург (Германия) през 1669 г. Бранд получава фосфор от сухия остатък на урината, но пази в тайна производствения процес. Той откри, че новото вещество има забележително свойство: то свети ярко в тъмното, след като е било изложено на светлина известно време. Бранд измисли много забавни трикове с фосфор и ги показа на приятелите си, печелейки добри пари от демонстрирането на тези експерименти. По-късно беше открито, че фосфорът е химичен елемент и получи името си.
Кобалтът е открит през 1737 г., а никелът - четиринадесет години по-късно. Кобалтовите и никеловите руди първоначално са били погрешни за медна руда и тъй като медта не може да бъде извлечена от тях, се е смятало, че в тези руди живеят зли духове. Оттам идват и имената им – кобалт (брауни) и купферникел (дяволска мед), които са оцелели и до днес.
Откриване на водорода
Получава се лесно чрез поставяне на парче метал в киселинен разтвор, като например солна киселина. Това освобождава водородни мехурчета. Фактът, че се образуват мехурчета, когато металът се спусне в киселина, е установен отдавна, но на никого не му е хрумвало, че освободеният газ е различен от другите известни газове.
И едва Хенри Кавендиш през 1766г. изследва свойствата на газа, получен при тази реакция, и го описва точно. Когато по-късно беше открито, че този газ, когато се изгори, образува вода, той беше наречен водород или произвеждащ вода (водород).
Откриване на азот и кислород
През 70-те години на 18 век много учени започват да провеждат експерименти с обикновен въздух, опитвайки се да открият от какво се състои.
Даниел Ръдърфорд откри, че горенето или дишането използва само част от даден обем въздух. Например, ако запалим свещ и я поставим в затворен съд, свещта ще гори известно време и след това ще угасне. По време на горенето част от въздуха се изразходва, а свещта отказва да изгори останалата част от него. Ако вместо свещ поставите мишка в съд, тя също ще изразходва част от въздуха и ще умре.
Ръдърфорд изследва газа, който остава, след като свещта изгасне или мишката спре да диша. Оказа се, че този газ е различен от обикновения въздух. Той не поддържа горене и животните не могат да живеят в него.
По същото време като Ръдърфорд редица други учени, а именно Джоузеф Пристли от Кавендиш и Карл Шееле, извършват подобна работа. Ръдърфорд обаче е първият, който точно описва азота. Ето защо Ръдърфорд се смята за откривател на азота.
Горе-долу през същия период много учени изследват другия основен компонент на въздуха – кислорода.
Пристли нагрява червен прах, живачен оксид, като фокусира лъч светлина върху него с леща и открива, че полученият газ поддържа горенето много ефективно. Така той открива кислорода.
Всъщност шведският химик Шееле извършва подобни експерименти, очевидно малко по-рано, но публикува работата си със закъснение.
Тогава известният френски учен Антоан Лавоазие изследва природата на горенето. Той показа, че когато метали като магнезий горят, те се свързват с кислород, увеличавайки теглото си. Това откритие е важен принос към химията.
По този начин броят на елементите познати на човекадо средата на 70-те години на 18 век достига двадесет.
Водород, Hydrogenium, H (1)Водородът е известен като горим (запалим) въздух от доста време. Получава се чрез действието на киселини върху метали; изгарянето и експлозиите на експлозивен газ са наблюдавани от Парацелз, Бойл, Лемери и други учени от 16-18 век. С разпространението на теорията за флогистона някои химици се опитаха да произведат водород като "свободен флогистон". В дисертацията на Ломоносов "За металния блясък" се описва получаването на водород чрез действието на "кисели алкохоли" (например "солен алкохол", т.е. солна киселина) за желязо и други метали; Руският учен е първият (1745 г.), който излага хипотезата, че водородът („запалима пара“ - пара inflammabilis) е флогистон. Кавендиш, който подробно изучава свойствата на водорода, излага подобна хипотеза през 1766 г. Той нарича водорода „запалим въздух“, получен от „метали“ (запалим въздух от метали), и вярва, както всички флогистици, че когато се разтвори в киселини металът губи вашия флогистон. Лавоазие, който през 1779 г. изследва състава на водата чрез нейния синтез и разлагане, нарича водород Hydrogine (водород) или Hydrogene (водород) от гръцки. хидро - вода и гейноме - произвеждам, раждам.
Номенклатурната комисия от 1787 г. приема думата производство Hydrogene от gennao - раждам. В Таблицата на простите тела на Лавоазие водородът се споменава сред петте (светлина, топлина, кислород, азот, водород) „прости тела, принадлежащи към трите царства на природата и които трябва да се разглеждат като елементи на телата“; Като стар синоним на името Hydrogene, Лавоазие нарича запалим газ (gaz inflammable), основата на запалимия газ. В руската химическа литература от края на 18 и началото на XIX V. Има два вида наименования на водорода: флогистичен (запалим газ, запалим въздух, възпламеним въздух, възпламеним въздух) и антифлогистичен (създание, създаващо вода, същество, създаващо вода, създаващ вода газ, водороден газ, водород). И двете групи думи са превод на френските имена на водород.
Водородните изотопи са открити през 30-те години на миналия век и бързо стават голяма стойноств науката и технологиите. В края на 1931 г. Urey, Brekwedd и Murphy изследват остатъка след дългосрочно изпаряване на течен водород и откриват тежък водород с атомно тегло 2. Този изотоп се нарича деутерий (D) от гръцки. - още един, втори. Четири години по-късно във вода, подложена на продължителна електролиза, е открит още по-тежък изотоп на водорода, 3H, наречен тритий (Tritium, T) от гръцки. - трети.
Хелий, Хелий, Той (2)
През 1868 г. френският астроном Янсен наблюдава пълно слънчево затъмнениеи спектроскопски изследва хромосферата на слънцето. Той открива ярко жълта линия в спектъра на слънцето, която той обозначава с D3, която не съвпада с жълтата D линия на натрия. По същото време същата линия в спектъра на слънцето е видяна от английския астроном Локиър, който разбира, че тя принадлежи на неизвестен елемент. Локиър, заедно с Франкланд, за когото работи тогава, решават да кръстят новия елемент хелий (от гръцкото helios - слънце). След това нова жълта линия беше открита от други изследователи в спектрите на „земните“ продукти; Така през 1881 г. италианецът Палмиери го открива, докато изучава газова проба, взета в кратера на Везувий. Американският химик Хилебранд, изучавайки уранови минерали, установи, че те отделят газове, когато са изложени на силна сярна киселина. Самият Хилебранд вярваше, че това е азот. Рамзи, който привлече вниманието към съобщението на Хилебранд, подложи на спектроскопски анализ газовете, отделени при обработката на минерала клевейт с киселина. Той откри, че газовете съдържат азот, аргон и неизвестен газ, който произвежда ярко жълта линия. Тъй като няма достатъчно добър спектроскоп, Рамзи изпраща проби от новия газ на Крукс и Локиър, които скоро идентифицират газа като хелий. Също през 1895 г. Рамзи изолира хелий от смес от газове; оказа се химически инертен като аргон. Скоро след това Локиър, Рунге и Пашен правят изявление, че хелият се състои от смес от два газа - ортохелий и парахелий; единият дава жълта спектрална линия, другият зелена. Те предложиха да нарекат този втори газ астерий (Asterium) от гръцки - звезда. Заедно с Травърс Рамзи тества това твърдение и доказа, че е погрешно, тъй като цветът на хелиевата линия зависи от налягането на газа.
Литий, литий, Li (3)
Когато Дейви провежда известните си експерименти върху електролизата на алкалоземни метали, никой не подозира за съществуването на литий. Литиевият алкалоземен метал е открит едва през 1817 г. от талантлив химик-аналитик, един от учениците на Берцелиус, Арфведсон. През 1800 г. бразилският минералог де Андрада Силва, по време на научно пътуване в Европа, открива два нови минерала в Швеция, които нарича петалит и сподумен, а първият от тях е преоткрит няколко години по-късно на остров Юте. Арфведсон се заинтересува от петалита, извърши пълен анализ на него и откри първоначално необяснима загуба на около 4% от веществото. Повтаряйки анализите по-внимателно, той установява, че петалитът съдържа „запалима основа от неизвестна досега природа“. Берцелиус предложи да го наречем литион, тъй като тази основа, за разлика от калия и содата, е открита за първи път в „царството на минералите“ (камъни); Това име произлиза от гръцки - камък. По-късно Арфведсън открива литиева пръст или литин в няколко други минерала, но опитите му да изолира свободния метал са неуспешни. Много малко количество метален литий е получено от Дейви и Бранде чрез електролиза на основа. През 1855 г. Бунзен и Матесен разработват промишлен метод за производство на метален литий чрез електролиза на литиев хлорид. В руската химическа литература от началото на 19 век. срещат се имена: литий, литин (Двигубски, 1826) и литий (Хес); литиевоземна (алкална) понякога се нарича литина.
Берилий, Be (4)
Минералите, съдържащи берилий (скъпоценни камъни) - берил, изумруд, изумруд, аквамарин и др., са известни от древността. Някои от тях са били добивани на Синайския полуостров още през 17 век. пр.н.е д. Стокхолмският папирус (3 век) описва методи за правене на фалшиви камъни. Името берил се среща на гръцки и латински (Beryll) антични писателии в древните руски произведения, например в „Сборника на Святослав“ от 1073 г., където берилът се появява под името вирулион. Изследването на химичния състав на ценните минерали от тази група обаче започва едва в края на 18 век. с настъпването на химико-аналитичния период. Първите анализи (Клапрот, Биндхайм и др.) не откриват нищо особено в берила. В края на 18в. известният минералог абат Гахуи обърна внимание на пълното сходство на кристалната структура на берила от Лимож и изумруда от Перу. Вокелин извършва химичен анализ на двата минерала (1797) и открива и в двата нова земя, различен от алуминия. След като получи солите на новата земя, той установи, че някои от тях имат сладък вкус, поради което нарече новата земя глюцина (Glucina) от гръцки. - сладко. Нов елемент, съдържащ се в тази земя, съответно е наречен глюциний (Glucinium). Това име е използвано във Франция през 19 век; Клапрот, като противник на именуване на нови елементи според произволни свойстватехните съединения, предложени да наричат глюциний берилий, като посочват, че съединенията на други елементи също имат сладък вкус. Металният берилий е получен за първи път от Wöhler и Bussy през 1728 г. чрез редуциране на берилиевия хлорид с метален калий. Нека отбележим тук изключителните изследвания на руския химик И. В. Авдеев върху атомното тегло и състава на берилиевия оксид (1842 г.). Авдеев установява атомното тегло на берилия като 9,26 (модерно 9,0122), докато Берцелиус го приема за 13,5 и правилната формула за оксида.
Има няколко версии за произхода на името на минерала берил, от който произлиза думата берилий. А. М. Василиев (според Diergart) цитира следното мнение на филолозите: латинските и гръцките имена на берил могат да бъдат сравнени с пракритската veluriya и санскритската vaidurya. Последното е името на определен камък и произлиза от думата vidura (много далеч), което изглежда означава някаква страна или планина. Мюлер предложи друго обяснение: vaidurya идва от оригиналния vaidarya или vaidalya, а последният от vidala (котка). С други думи, vaidurya означава грубо "котешко око". Рай посочва, че на санскрит топазът, сапфирът и коралът се смятат за котешко око. Третото обяснение е дадено от Липман, който смята, че думата берил означава някакъв вид северна страна(откъдето идват скъпоценните камъни) или хората. На друго място Липман отбелязва, че Николай Кузански пише, че немското Brille (очила) идва от варварското латинско berillus. И накрая, Lemery, обяснявайки думата берил (Beryllus), посочва, че Berillus или Verillus означава "човешки камък".
В руската химическа литература от началото на 19 век. Глюцина се нарича сладка земя, сладка земя (Севергин, 1815), сладка земя (Захаров, 1810), глутина, глицин, основата на глицинова земя, а елементът се нарича глициния, глицинит, глиций, сладка земя и т.н. Giese предложи името берилий (1814 г.). Хес обаче се придържа към името Glitium; той също е използван като синоним от Менделеев (1-во издание „Основи на химията“).
Бор, Борум, V (5)
Естествените борни съединения (английски Boron, френски Bore, немски Bor), главно нечист боракс, са известни от ранно средновековие. Под имената Тинкал, Тинкар, Атинкар (Tinkal, Tinkar, Attinkar) бораксът е внесен в Европа от Тибет; използван е за спояване на метали, особено злато и сребро. В Европа тинкалът е наричан по-често боракс (Borax) от арабската дума bauraq и персийската дума burah. Понякога означаваше боракс или борако различни вещества, например сода (нитрон). Руланд (1612) нарича боракс хризокола, смола, способна да „слепва“ злато и сребро. Lemery (1698) също нарича боракса „златно лепило“ (Auricolla, Chrisocolla, Gluten auri). Понякога боракс означаваше нещо като „юзда от злато“ (capistrum auri). В александрийската, елинистическата и византийската химическа литература бор и борахон, както и на арабски (баурак) обикновено означават алкали, например баурак арман (арменски борак) или сода, по-късно започват да наричат боракс.
През 1702 г. Хомберг, чрез калциниране на боракс с железен сулфат, получава "сол" (борна киселина), която става известна като "успокояващата сол на Хомберг" (Sal sedativum Hombergii); тази сол се използва широко в медицината. През 1747 г. Барон синтезира боракс от "успокояваща сол" и натрон (сода). Съставът на боракса и „солта“ обаче остава неизвестен до началото на 19 век. Химическата номенклатура от 1787 г. съдържа името horacique acid (борна киселина). Лавоазие в своята „Таблица на простите тела” цитира радикален борак. През 1808 г. Gay-Lussac и Thénard успяват да изолират свободния бор от борния анхидрид чрез нагряване на последния с метален калий в медна тръба; те предложиха елементът да се нарича бор (Бора) или бор (Бор). Дейви, който повтори експериментите на Гей-Люсак и Тенар, също получи свободен бор и го нарече бораций. По-късно британците съкратиха това име до Бор. В руската литература думата боракс се среща в сборници с рецепти от 17-18 век. В началото на 19в. Руските химици наричат борборакс (Захаров, 1810), бурон (Страхов, 1825), основа на борна киселина, бурацин (Севергин, 1815), бория (Двигубски, 1824). Преводачът на книгата на Giese нарича бор бурий (1813). Освен това има имена като бормашина, брана, буронит и др.
Въглерод, Карбонеум, С (6)
Въглеродът (английски Carbon, френски Carbone, немски Kohlenstoff) под формата на въглища, сажди и сажди е познат на човечеството от незапомнени времена; преди около 100 хиляди години, когато нашите предци са владеели огъня, те са се занимавали с въглища и сажди всеки ден. Вероятно много рано хората са се запознали с алотропните модификации на въглерода - диамант и графит, както и изкопаемите въглища. Не е изненадващо, че изгарянето на вещества, съдържащи въглерод, е един от първите химични процеси, които интересуват човека. Тъй като горящото вещество изчезва, когато се погълне от огън, горенето се счита за процес на разлагане на веществото и следователно въглищата (или въглеродът) не се считат за елемент. Елементът беше огънят - явление, съпътстващо горенето; В древните учения за елементите огънят обикновено се появява като един от елементите. включено началото на XVII- XVIII век Възниква теорията за флогистона, представена от Бехер и Стал. Тази теория признава наличието във всяко горимо тяло на специално елементарно вещество - безтегловна течност - флогистон, която се изпарява по време на процеса на горене. Тъй като когато се изгори голямо количество въглища, остава само малко пепел, флогистиката смята, че въглищата са почти чист флогистон. Това е, което обяснява, по-специално, "флогистичния" ефект на въглищата - способността му да възстановява метали от "вар" и руди. По-късните флогистици - Реомюр, Бергман и други - вече започват да разбират, че въглищата са елементарно вещество. „Чистите въглища“ обаче са признати за първи път от Лавоазие, който изучава процеса на изгаряне на въглища и други вещества във въздух и кислород. В книгата на Guiton de Morveau, Lavoisier, Berthollet и Fourcroix „Метод на химическата номенклатура“ (1787) името „въглерод“ (carbone) се появява вместо френското „чисти въглища“ (charbone pur). Под същото име въглеродът се появява в „Таблицата на простите тела“ в „Елементарния учебник по химия“ на Лавоазие. През 1791 г. английският химик Тенант е първият, който получава свободен въглерод; той прекарва фосфорни пари върху калцинирана креда, което води до образуването на калциев фосфат и въглерод. Отдавна е известно, че при силно нагряване диамантът гори, без да оставя следи. Още през 1751 г. френският крал Франциск I се съгласява да даде диамант и рубин за експерименти с изгаряне, след което тези експерименти дори стават модерни. Оказа се, че само диамантът гори, а рубинът (алуминиев оксид с примес на хром) може да издържи продължително нагряване във фокуса на лещата за запалване без повреда. Комплект Lavoisier нов опитпри изгаряне на диамант с голяма запалителна машина и стигна до заключението, че диамантът е кристален въглерод. Вторият алотроп на въглерода - графит - в алхимичния период се счита за модифициран оловен блясък и се нарича plumbago; Едва през 1740 г. Пот открива липсата на оловни примеси в графита. Шееле изучава графита (1779) и като флогистик го смята за специален вид сярно тяло, специален минерален въглен, съдържащ свързана „въздушна киселина“ (CO2) и голямо количество флогистон.
Двадесет години по-късно Guiton de Morveau превръща диаманта в графит и след това във въглена киселина чрез внимателно нагряване.
Международното име Carboneum идва от лат. карбо (въглища). Думата е много древен произход. Сравнява се с cremare – изгарям; корен car, cal, руски гар, гал, гол, санскрит sta означава варя, готвя. Думата "карбо" се свързва с имената на въглерод в други европейски езици(въглерод, въглен и др.). Немският Kohlenstoff идва от Kohle - въглища (старонемски kolo, шведски kylla - загрявам). Староруският угорати, или угарати (да горя, изгарям) има корен гар, или планини, с възможен преход към гол; въглища в староруски югал или въглища от същия произход. Думата диамант (Diamante) произлиза от старогръцки - неразрушим, непреклонен, твърд, а графит от гръцки - пиша.
В началото на 19в. старата дума въглища в руската химическа литература понякога се заменя с думата "карбонат" (Scherer, 1807; Severgin, 1815); От 1824 г. Соловьов въвежда името въглерод. 

Азот, Nitrogenium, N (7)
Азотът (английски Nitrogen, френски Azote, немски Stickstoff) е открит почти едновременно от няколко изследователи. Кавендиш получава азот от въздуха (1772), като го прекарва през горещи въглища и след това през алкален разтвор, за да абсорбира въглероден диоксид. Кавендиш не дава специално име на новия газ, наричайки го мефитичен въздух (Air mephitic от лат. mephitis - задушаващо или вредно изпарение на земята). Пристли скоро откри, че ако свещ гори във въздуха дълго време или присъства животно (мишка), тогава такъв въздух става неподходящ за дишане. Официално откриването на азота обикновено се приписва на ученика на Блек, Ръдърфорд, който през 1772 г. публикува дисертация (за степента на доктор по медицина) - „За неподвижния въздух, иначе наричан задушаващ“, където някои от химичните свойства на азота бяха описани за първи път. През същите тези години Шееле получава азот от атмосферен въздухпо същия начин като Кавендиш. Той нарече новия газ „развален въздух“ (Verdorbene Luft). Тъй като преминаването на въздух през горещи въглища се смяташе от химиците флогистици за флогистициране, Priestley (1775) нарече азот флогистиран въздух. Кавендиш също говори по-рано за флогистиката на въздуха в своя опит. Лавоазие през 1776-1777 г изследва подробно състава на атмосферния въздух и установи, че 4/5 от неговия обем се състои от задушаващ газ (Air mofette - атмосферен мофет или просто Mofett). Имената на азота - флогистиран въздух, мефичен въздух, атмосферен мофет, развален въздух и някои други - бяха използвани преди признаването на нова химическа номенклатура в европейските страни, т.е. преди публикуването на известната книга „Методът на химическата номенклатура ” (1787).
Съставителите на тази книга - членове на номенклатурната комисия на Парижката академия на науките - Guiton de Morveau, Lavoisier, Berthollet и Fourcroix - приеха само няколко нови имена за прости вещества, по-специално имената "кислород" и "водород". предложен от Лавоазие. При избора на ново име за азота комисията, основана на принципите на кислородната теория, се оказа затруднена. Както е известно, Лавоазие предложи да даде прости веществаимена, които биха отразявали основните им химични свойства. Съответно на този азот трябва да се даде името „азотни радикали“ или „нитратни радикали“. Такива имена, пише Лавоазие в книгата си "Принципи на елементарната химия" (1789), се основават на старите термини селитра или селитра, приети в изкуствата, в химията и в обществото. Те биха били доста подходящи, но е известно, че азотът е и основата на летливия алкален (амоняк), както наскоро бе открил Бертоле. Следователно наименованието радикал или основа на нитратна киселина не отразява основното химични свойстваазот. Не е ли по-добре да се спрем на думата азот, която според членовете на номенклатурната комисия отразява основното свойство на елемента – непригодността му за дишане и живот? Авторите на химическата номенклатура предложиха да изведат думата азот от гръцкия отрицателен префикс "а" и думата живот. По този начин името азот, според тях, отразява неговата нежизненост или безжизненост.
Думата азот обаче не е измислена от Лавоазие или неговите колеги от комисията. Той е известен от древни времена и е използван от философи и алхимици от Средновековието за обозначаване на „първичната материя (основа) на металите“, така наречения живак на философите или двойния живак на алхимиците. Думата азот навлиза в литературата вероятно през първите векове на Средновековието, подобно на много други зашифровани имена с мистично значение. Среща се в трудовете на много алхимици, като се започне от Бейкън (XIII век) - у Парацелз, Либавий, Валентин и други дори посочва, че думата азот (азот) идва от древната испано-арабска дума azoque (. azoque или azoc), което означава живак. Но по-вероятно е тези думи да са се появили в резултат на писани изкривявания на корена на думата азот (азот или азот). Сега произходът на думата азот е установен по-точно. Древните философи и алхимици са смятали „първичната материя на металите” за алфа и омега на всичко, което съществува. От своя страна този израз е заимстван от Апокалипсиса - последната книга на Библията: „Аз съм алфата и омегата, началото и краят, първият и последният.“ В древността и през Средновековието християнските философи смятат за правилно да използват само три езика, които са признати за „свещени“, когато пишат своите трактати - латински, гръцки и иврит (надписът на кръста при разпъването на Христос, според евангелската история е направено на тези три езика). За да се образува думата азот, бяха взети началните и крайните букви от азбуката на тези три езика (a, alpha, aleph и zet, omega, tov - AAAZOT).
Съставителите на новата химическа номенклатура от 1787 г. и най-вече инициаторът за нейното създаване Гитон дьо Морво са били наясно със съществуването на думата азот от древни времена. Морво отбеляза в "Методическата енциклопедия" (1786) алхимичното значение на този термин. След публикуването на Метода на химическата номенклатура, противниците на кислородната теория - флогистиката - остро критикуват новата номенклатура. Особено, както отбелязва самият Лавоазие в своя учебник по химия, приемането на „древни имена“ беше критикувано. По-специално La Mettrie, издател на списанието Observations sur la Physique, крепост на противниците на кислородната теория, посочи, че думата азот е използвана от алхимиците в различен смисъл.
Въпреки това новото име беше прието във Франция, както и в Русия, заменяйки приетите преди това наименования „флогистиран газ“, „мофет“, „мофетова основа“ и др.
Словообразуването азот от гръцки също предизвика справедливи коментари. Д. Н. Прянишников в книгата си „Азотът в живота на растенията и в селското стопанство на СССР“ (1945 г.) съвсем правилно отбелязва, че словообразуването от гръцки „повдига съмнения“. Очевидно и съвременниците на Лавоазие са имали тези съмнения. Самият Лавоазие в своя учебник по химия (1789 г.) използва думата азот заедно с името „нитричен радикал“.
Интересно е да се отбележи, че по-късните автори, очевидно опитвайки се по някакъв начин да оправдаят неточността, допусната от членовете на номенклатурната комисия, извеждат думата азот от гръцки - животворящ, животворящ, създавайки изкуствената дума "azotikos", която е отсъства в гръцки(Диргарт, Реми и др.). Този начин на образуване на думата азот обаче едва ли може да се счита за правилен, тъй като производната дума за името азот би трябвало да звучи „азотикон“.
Неадекватността на името азот беше очевидна за много от съвременниците на Лавоазие, които напълно симпатизираха на неговата кислородна теория. Така Чаптал в своя учебник по химия „Елементи на химията“ (1790 г.) предлага думата азот да се замени с думата азот (азот) и нарича газ, в съответствие с възгледите на своето време (всяка газова молекула е представена като заобиколена чрез калорична атмосфера), „азот“ (Gas nitrogene). Чаптал подробно мотивира предложението си. Един от аргументите беше указанието, че името, което означава безжизнен, може с по-голямо основание да се даде на други прости тела (притежаващи например силни отровни свойства). Името азот, прието в Англия и Америка, по-късно става основа за международното име на елемента (Nitrogenium) и символа за азот - N. Във Франция в началото на 19в. Вместо символа N е използван символът Az. През 1800 г. един от съавторите на химическата номенклатура, Fourcroy, предлага друго име - алкалиген, въз основа на факта, че азотът е „основата“ на летливия алкален (Alcali volatil) - амоняк. Но това име не е прието от химиците. Нека накрая да споменем името азот, което се използва от химиците флогистици и по-специално от Пристли в края на 18 век. - септон (Septon от френския Septique - гнилостен). Това име очевидно е предложено от Мичъл, ученик на Блек, който по-късно работи в Америка. Дейви отхвърли това име. В Германия от края на 18 век. и до днес азотът се нарича Stickstoff, което означава "задушаващо вещество".
Що се отнася до старите руски наименования на азота, които се появяват в различни произведения от края на 18 - началото на 19 век, те са както следва: задушлив газ, нечист газ; мофетичен въздух (всички това са преводи на френското име Gas mofette), задушаващо вещество (превод на немското Stickstoff), флогистичен въздух, раздразнен, засегнат въздух (флогистичните имена са превод на термина, предложен от Пристли - Плогистичен въздух). Използвани са и имена; развален въздух (превод на термина на Шееле Verdorbene Luft), селитра, газ от селитра, азот (превод на името, предложено от Chaptal - азот), алкалиген, алкали (термините на Fourcroy, преведени на руски през 1799 и 1812 г.), септон, гнилостен агент (Septon ) и т.н. Наред с тези многобройни имена се използват и думите азот и азотен газ, особено от началото на 19 век.
В. Севергин в своето „Ръководство за най-удобно разбиране на чуждестранни химически книги“ (1815) обяснява думата азот по следния начин: „Azoticum, Azotum, Azotozum - азот, задушаващо вещество“; "Азот - Азот, селитра"; "нитратен газ, азотен газ." Думата азот най-накрая влезе в руската химическа номенклатура и измести всички други имена след публикуването на „Основи на чистата химия“ от Г. Хес (1831).
Производните имена на съединения, съдържащи азот, се формират на руски и други езици или от думата азот (азотна киселина, азосъединения и др.), Или от международното наименование азот (нитрати, нитросъединения и др.). Последният термин произлиза от древните имена nitr, nitrum, nitron, които обикновено означават селитра, понякога естествена сода. В речника на Руланд (1612) се казва: "Nitrum, boron (baurach), селитра (Sal petrosum), nitrum, сред германците - Salpeter, Bergsalz - същото като Sal petrae."
 |
Кислород, Oxygenium, O (8)
Откриването на кислорода (английски Oxygen, френски Oxygene, немски Sauerstoff) бележи началото на съвременния период в развитието на химията. От древни времена е известно, че за горенето е необходим въздух, но в продължение на много векове процесът на горене остава неясен. Едва през 17в. Мейоу и Бойл независимо изразиха идеята, че въздухът съдържа някакво вещество, което поддържа горенето, но тази напълно рационална хипотеза не беше развита тогава, тъй като идеята за горенето като процес на комбиниране на горящо тяло с определен неразделна частвъздух, изглеждаше по това време в противоречие с такъв очевиден факт като факта, че по време на горенето се извършва разлагането на горящото тяло на елементарни компоненти. Именно на тази основа в началото на 17в. Възниква теорията за флогистона, създадена от Бехер и Щал. С настъпването на химико-аналитичния период в развитието на химията (втората половина на 18 век) и появата на "пневматичната химия" - един от основните клонове на химико-аналитичната посока - горенето, както и дишането , отново привлече вниманието на изследователите. Откриването на различни газове и установяването на тяхната важна роля в химичните процеси е един от основните стимули за систематичните изследвания на процесите на горене, предприети от Лавоазие. Кислородът е открит в началото на 70-те години на 18 век. Първият доклад за това откритие е направен от Пристли на среща на Кралското общество на Англия през 1775 г. Пристли, чрез нагряване на червен живачен оксид с голяма горяща чаша, получава газ, в който свещта гори по-ярко, отколкото в обикновен въздух, и тлеещата треска пламна. Пристли определя някои от свойствата на новия газ и го нарича дафлогистичен въздух. Въпреки това, две години по-рано, Priestley (1772) Scheele също получава кислород чрез разлагане на живачен оксид и други методи. Шееле нарича този газ огън въздух (Feuerluft). Шееле успява да съобщи за откритието си едва през 1777 г. Междувременно през 1775 г. Лавоазие говори пред Парижката академия на науките със съобщение, че е успял да получи „най-чистата част от въздуха, който ни заобикаля“, и описва свойствата на тази част от въздуха. Първоначално Лавоазие нарече този „въздух“ витален (Air empireal, Air vital), основата на жизнения въздух (Base de l'air vital) откриването на кислорода е почти едновременно различни държавипредизвика полемика относно приоритета. Пристли беше особено упорит в търсенето на признание като откривател. По същество тези спорове още не са приключили. Подробно изследване на свойствата на кислорода и неговата роля в процесите на горене и образуването на оксиди доведе Лавоазие до неправилното заключение, че този газ е киселинообразуващ принцип. През 1779 г. Лавоазие, в съответствие с това заключение, въвежда ново име за кислорода - принципът на образуване на киселина (principe acidifiant ou principe oxygine). Лавоазие извежда думата oxygine, която се появява в това сложно име, от гръцки. - киселина и „произвеждам“.
Флуор, флуор, F (9)
Флуорът (английски Fluorine, френски и немски Fluor) е получен в свободно състояние през 1886 г., но неговите съединения са известни отдавна и са широко използвани в металургията и производството на стъкло. Първото споменаване на флуорит (CaF2) под името флуорит (Fliisspat) датира от 16 век. Едно от произведенията, приписвани на легендарния Василий Валентин, споменава боядисани в различни цветове камъни - флюс (Fliisse от лат. fluere - теча, изливам), които са били използвани като флюсове при топенето на метали. Агрикола и Либавий пишат за това. Последният въвежда специални наименования за този флюс - флуорипат (Flusspat) и минерални флуори. Много автори на химични и технически произведения от 17-ти и 18-ти век. описвам различни видовефлуорипат. В Русия тези камъни се наричаха перка, палта, плюнка; Ломоносов класифицира тези камъни като селенити и ги нарича шпат или флюс (кристален флюс). Руските майстори, както и колекционерите на колекции от минерали (например през 18 век княз П. Ф. Голицин) знаеха, че някои видове шпат при нагряване (например в топла вода) светят в тъмното. Но Лайбниц в своята история на фосфора (1710) споменава термофосфора (Thermophosphorus) в това отношение.
Очевидно химиците и занаятчиите химици са се запознали с флуороводородна киселина не по-късно от 17 век. През 1670 г. нюрнбергският занаятчия Шванхард използва флуорипат, смесен със сярна киселина, за да гравира шарки върху стъклени чаши. По това време обаче природата на флуорипат и флуороводородна киселина беше напълно неизвестна. Смятало се е например, че силициевата киселина има ецващ ефект в процеса на Шванхард. Това погрешно мнение беше елиминирано от Шееле, който доказа, че когато флуорипатът реагира със сярна киселина, се получава силициева киселина в резултат на корозията на стъклена реторта от получената флуороводородна киселина. В допълнение, Шееле установява (1771), че флуорият шпат е комбинация от варовита пръст със специална киселина, наречена „шведска киселина“. Лавоазие разпозна радикала на флуороводородна киселина като просто тяло и го включи в своята таблица с прости тела. В повече или по-малко чиста форма, флуороводородна киселина е получена през 1809 г. от Gay-Lussac и Thénard чрез дестилация на флуор шпат със сярна киселина в оловна или сребърна реторта. По време на тази операция и двамата изследователи са били отровени. Истинската природа на флуороводородна киселина е установена през 1810 г. от Ампер. Той отхвърли мнението на Лавоазие, че флуороводородна киселина трябва да съдържа кислород, и доказа аналогията на тази киселина със солната киселина. Ампер докладва откритията си на Дейви, който наскоро установи елементарната природа на хлора. Дейви напълно се съгласи с аргументите на Ампер и похарчи много усилия за получаване на свободен флуор чрез електролиза на флуороводородна киселина и други начини. Като се има предвид силното разяждащо действие на флуороводородна киселина върху стъклото, както и върху растителните и животинските тъкани, Ампер предлага елементът, съдържащ се в него, да се нарече флуор (на гръцки - унищожение, смърт, мор, чума и др.). Дейви обаче не приема това наименование и предлага друго - Флуор, по аналогия с тогавашното наименование на хлора - Хлор, двете имена все още се използват в английски. На руски език е запазено името, дадено от Ампер.
Многобройни опити за изолиране на свободен флуор през 19 век. не доведе до успешни резултати. Едва през 1886 г. Мойсан успява да направи това и да получи свободен флуор под формата на жълто-зелен газ. Тъй като флуорът е необичайно агресивен газ, Мойсан трябваше да преодолее много трудности, преди да намери материал, подходящ за оборудване при експерименти с флуор. U-образната тръба за електролиза на флуороводородна киселина при минус 55oC (охлаждана с течен метилхлорид) е направена от платина с тапи от флуор шпат. След изследване на химичните и физичните свойства на свободния флуор, той намира широко приложение. Сега флуорът е един от основни компонентисинтез на широка гама от органофлуорни вещества. В руската литература от началото на 19 век. флуорът се нарича по различен начин: основа на флуороводородна киселина, флуорин (Двигубски, 1824), флуорност (Йовски), флуор (Шчеглов, 1830), флуор, флуор, флуорид. Хес въвежда името флуор през 1831 г.
Неон, Неон, Не (10)
Този елемент е открит от Рамзи и Травърс през 1898 г., няколко дни след откриването на криптона. Учените са взели проби от първите мехурчета газ, получени от изпарението на течен аргон, и са открили, че спектърът на този газ показва наличието на нов елемент. Рамзи говори за избора на име за този елемент:
„Когато за първи път разгледахме неговия спектър, моят 12-годишен син беше там.
"Татко", каза той, "как е името на този красив газ?"
„Все още не е решено“, отговорих аз.
- Ново ли е? - полюбопитствал синът.
— Новооткрито — възразих аз.
- Защо не го наречете Новум, татко?
„Това не важи, защото novum не е гръцка дума“, отговорих аз. - Ще го наречем неон, което означава нов на гръцки.
Ето как газът получи името си."
Автор: Figurovsky N.A.
Химия и химици №1 2012г
Следва продължение...
Официално са добавени четири нови химически елемента периодична таблицаМенделеев. Така нейният седми ред беше завършен. Новите елементи - 113, 115, 117 и 118 - са синтезирани изкуствено в лаборатории в Русия, САЩ и Япония (т.е. не съществуват в природата). Въпреки това, официалното признаване на откритията, направени от група независими експерти, трябваше да изчака до края на 2015 г.: Международният съюз по чиста и приложна химия обяви попълването на 30 декември 2015 г.
Всички "нови" елементи бяха синтезирани в лабораторни условияизползвайки по-леки атомни ядра. В добрите стари времена беше възможно да се изолира кислород чрез изгаряне на живачен оксид - но сега учените трябва да прекарат години и да използват масивни ускорители на частици, за да открият нови елементи. В допълнение, нестабилни агломерации от протони и неутрони (така изглеждат новите елементи за учените) се слепват само за част от секундата, преди да се разпаднат на по-малки, но по-стабилни „фрагменти“.
Сега отбори, които са получили и доказали съществуването на нови елементи от таблицата, имат право да предложат нови имена за тези елементи, както и две буквени символи, за да ги обозначат.
Елементите могат да бъдат кръстени на едно от техните химически или физически свойства, както и по име на минерал, топоним или учен. Името може също да се основава на митологични имена.
В момента елементите имат дисонансни работни наименования - унунтрий (Uut), унунпентиум (Uup), унунсептиум (Uus) и унунокций (Uuo) - които съответстват на латинските наименования на цифрите в техния номер.
113-ият елемент е даден на изследователи от Япония. Този елемент вероятно ще бъде първият създаден от човека елемент, кръстен на държава Източна Азия. Когато елементът беше открит за първи път преди 12 години, беше предложено да се нарече японий.
За първи път екип от института обяви откритието на елемент 113 природни науки RIKEN в Уако и убедителни доказателства бяха предоставени през 2012 г. По това време японски специалисти са създали три атома на елемента. Тогава руски и американски изследователи също повториха експеримента.
Въпреки факта, че учени от Русия и Съединените щати не са получили правото да измислят име за елемент 113, те могат да назоват други елементи. Elements и бяха създадени за първи път благодарение на сътрудничеството на United Institute ядрени изследванияв Дубна (Русия), Националната лаборатория на Лорънс Ливърмор в Лорънс Ливърмор, Калифорния и Националната лаборатория Оук Ридж в Тенеси. Между другото, вече е направено предложение 117-ият елемент да се нарече „Московия“.
Съществуването на елемент 115 е потвърдено от експериментите на шведски учени, работещи с немски ускорител. Екипът от Дубна и Ливърмор е признат за откривател на елемента – най-тежкият създаван някога. Историята на синтеза на този елемент е доста сложна - успешни експерименти бяха докладвани през 1999 г., но две години по-късно резултатите бяха признати за фалшификация.
Нека добавим, че физиците работят в момента. Учените смятат, че с помощта модерни технологиинай-накрая ще стане възможно. Изследователи от Центъра за изследване на тежки йони Хелмхолц обаче работиха върху създаването на 120-ия елемент в продължение на пет месеца през 2012 г., но техните експерименти не бяха успешни. Някои експерти смятат, че шансовете за получаване на 120-ия елемент са невероятно малки.